18: Divertículos, anomalías del uraco y utrículos
Este capítulo durará aproximadamente 25 minutos para leer.
Anomalías del uraco
Embriología y Anatomía
El úraco es una estructura tubular que conecta el alantoides a nivel del ombligo con la cúpula de la vejiga y permanece permeable durante la gestación.1 La luz normalmente se cierra alrededor de la duodécima semana de gestación y se oblitera por completo. Tras la obliteración, lo que típicamente permanece es un cordón fibroso que se extiende desde el aspecto inferior del ombligo hasta la cúpula de la vejiga. El úraco es extraperitoneal y se visualiza fácilmente durante la visualización laparoscópica de la pelvis (Figura 1).
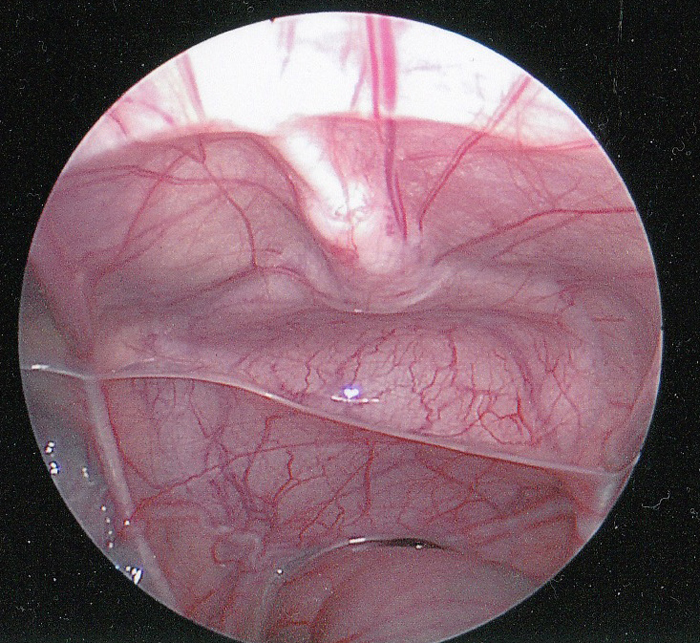
Figura 1 Vista laparoscópica intraperitoneal del uraco. El cordón fibroso del uraco (ligamento umbilical medio) se muestra en la línea media extendiéndose hasta la cúpula de la vejiga. El recto se encuentra inferiormente. Se puede observar el conducto deferente extendiéndose lateralmente justo por encima del recto.
El uraco está cubierto por los pliegues del peritoneo para formar el ligamento umbilical medio. En raras ocasiones, el uraco puede presentar discontinuidades en el cordón fibroso o incluso obliteración completa del cordón. Es un reparo quirúrgico importante para marcar la cúpula vesical y garantizar la correcta colocación de una vesicostomía.
Clasificación de las anomalías uracales
Las anomalías del uraco se deben a la falta de obliteración completa de la luz durante la gestación.2 Su clasificación anatómica se basa en el grado en que ha persistido la permeabilidad del uraco y varía desde la permeabilidad completa con libre flujo de orina hasta un pequeño trayecto sinusal ciego que se origina en la piel (Figura 2). Un quiste uracal puede estar presente en cualquier localización a lo largo del trayecto del uraco, pero se encuentra con mayor frecuencia cerca de la cúpula vesical. Un divertículo uracal—la anomalía más rara descrita—es una permeabilidad parcial del uraco que drena hacia la cúpula de la vejiga.
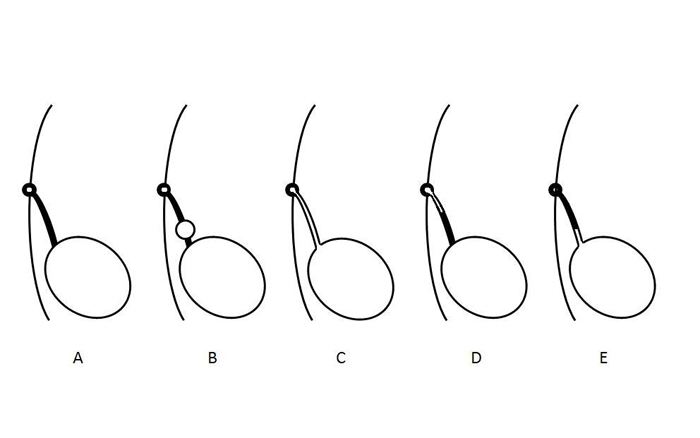
Figura 2 Diagrama que ilustra diferentes tipos de anomalías del uraco. A- Obliteración normal de la luz del uraco. B- Quiste uracal. C- Uraco permeable. D- Seno uracal. E- Divertículo uracal. Estas anomalías no son mutuamente excluyentes y pueden presentarse en combinación.
La incidencia relativa de los diferentes tipos de anomalías del uraco de varias series clínicas se muestra en Tabla 1.3,4,5,6,7,8,9
Tabla 1 Resumen de los tipos e incidencia de las anomalías del uraco que se presentan en niños.
| Autor | # Pacientes | Quiste | Permeable | Seno | Divertículo |
|---|---|---|---|---|---|
| Naiditch | 103 | 38 | 21 | 11 | 13 |
| Fox | 66 | 34 | 14 | 7 | 10 |
| Ashley | 46 | 25 | 6 | 14 | 1 |
| Cilento | 45 | 16 | 7 | 22 | 0 |
| Rich | 35 | 12 | 19 | 4 | 0 |
| Yiee | 31 | 19 | 7 | 5 | 0 |
| Copp | 29 | 7 | 3 | 17 | 2 |
| Total | 355 | 151 (43) | 108 (30) | 80 (23) | 26 (7) |
Resulta interesante que exista un único reporte de caso de un uraco permeable que se cerró espontáneamente con 2 semanas de drenaje mediante catéter y persistió como un divertículo uracal.10
Presentación clínica
Los síntomas de presentación más comunes en niños con anomalías del uraco son la secreción umbilical que persiste semanas después del parto o una masa y/o dolor por infección.3,6,8,11 La secreción umbilical puede ser clara, serosa, purulenta o sanguinolenta y orienta hacia su causa: la fuga persistente de líquido claro (probablemente orina) en un lactante sugiere un uraco permeable, mientras que un líquido turbio, seroso o sanguinolento es indicativo de un seno uracal o un quiste uracal. Existe una distribución etaria bimodal con presentación a una media de 1-3 meses de edad en aquellos con seno uracal o permeabilidad del uraco, frente a los 3 años en quienes se presentan con un quiste uracal.8 El diagnóstico diferencial de la secreción umbilical también incluye onfalitis, remanente del conducto onfalomesentérico o un granuloma umbilical.6
Tabla 2 Síntomas de presentación en niños con anomalías del uraco.
| Autor | N.º de pacientes | Drenaje | Masa/Infección | Dolor | Asintomático | Otros |
|---|---|---|---|---|---|---|
| Gleason | 721 | 26 | 19 | 17 | 667 | 0 |
| Naiditch | 103 | 60 | 7 | 4 | 18 | 12 |
| Stopak | 85 | 43 | 36 | 0 | 4 | 1 |
| Dethlefs | 68 | 52 | 32 | 0 | 8 | 0 |
| Cilento | 45 | 19 | 15 | 10 | 0 | 1 |
| Yiee | 37 | 20 | 8 | 4 | 2 | 3 |
| Total | 1059 | 220 (21) | 117 (11) | 35 (3) | 699 (66) | 17 (2) |
El examen físico también puede ser útil. Un uraco permeable o un seno uracal pueden aparecer como un hoyuelo o una depresión en la base del ombligo (Figura 3).
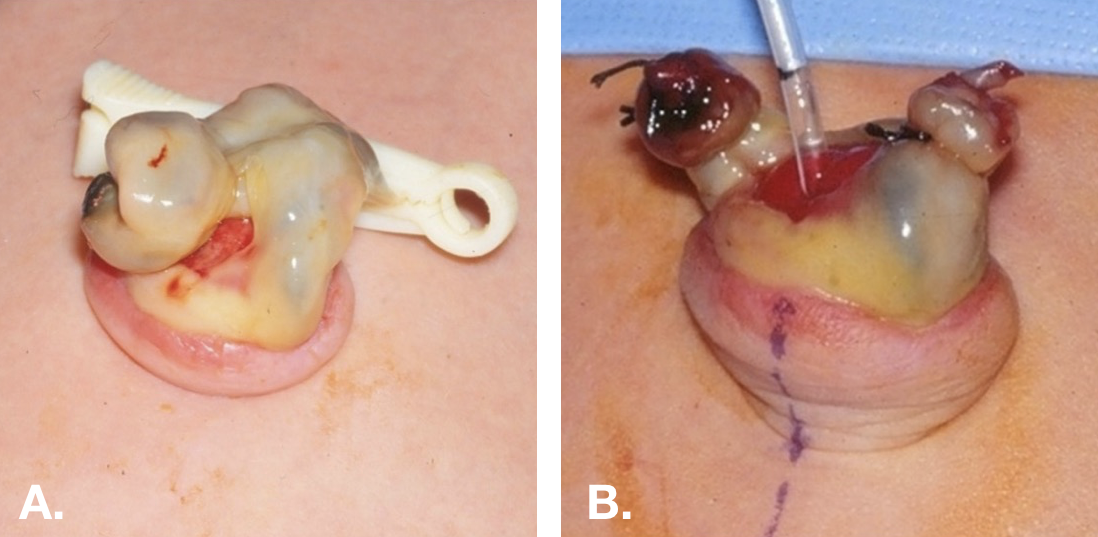
Figura 3 Uraco permeable en un recién nacido. A. Muestra el aspecto rojo intenso del extremo umbilical de un uraco permeable. B. La piel umbilical se ha evertido y se ha pasado una pequeña sonda de alimentación a través del uraco permeable hasta la vejiga.
Algunas anomalías del uraco se detectan de forma incidental durante la evaluación radiológica de rutina de otros trastornos, como las infecciones del tracto urinario o la hidronefrosis prenatal. Los quistes uracales suelen observarse durante la ecografía de la vejiga (Figura 4).
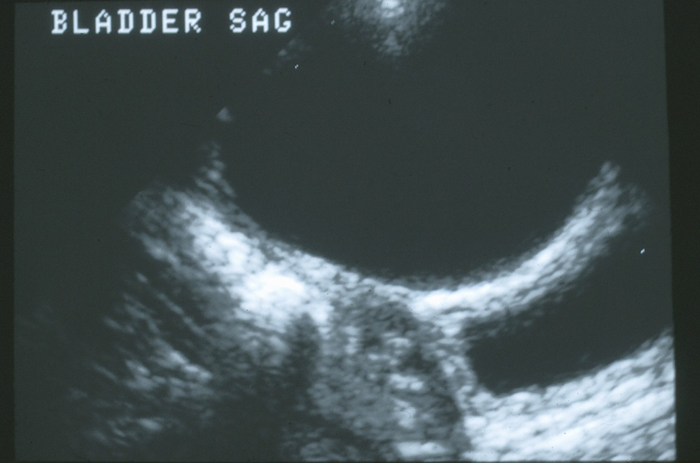
Figura 4 Vista sagital de la cúpula de la vejiga en la línea media. Hay un gran quiste uracal anecoico anterior a la pared vesical.
Carcinoma del uraco
Dado que el carcinoma del uraco no es una enfermedad de la que se haya informado que se presente en niños o adolescentes, el tratamiento de este trastorno no se incluirá en este capítulo.5,12 Como se discutirá en la sección sobre el manejo, se desconocen el riesgo de que una anomalía del uraco asintomática desarrolle carcinoma y, por lo tanto, el valor de la escisión profiláctica. Los factores de riesgo de carcinoma en una anomalía del uraco incluyen un tamaño mayor de 4 cm y edad > 55 años. Las calcificaciones son un hallazgo frecuente en el carcinoma; sin embargo, se desconoce el significado de las calcificaciones en un remanente benigno del uraco asintomático.5,12 Parecería prudente extirpar las lesiones con calcificaciones, dado que las calcificaciones pueden asociarse con inflamación crónica, la cual se asocia con la carcinogénesis.
Evaluación radiológica
Los estudios de imagen se guían por los síntomas de presentación y el grado de sospecha clínica.6,8 Un uraco permeable que permite el drenaje libre de orina a través del ombligo puede visualizarse con alta sensibilidad mediante una cistouretrografía miccional (VCUG) o un sinograma. Tradicionalmente se realizaba una VCUG para identificar el uraco permeable y también proporcionar una evaluación anatómica de la vejiga y evaluar la obstrucción de la salida vesical o el reflujo vesicoureteral (Figura 5). Sin embargo, la ecografía abdominal es adecuada para el diagnóstico en la mayoría de los pacientes, está más ampliamente disponible, es menos invasiva y menos costosa; por lo tanto, se ha convertido en el estándar para el diagnóstico, y la VCUG se reserva para los casos complicados.3,13 Es importante notificar al ecografista sobre la sospecha clínica de anomalía uracal para que se examine minuciosamente la pared abdominal en la línea media. Los quistes uracales infectados aparecen como grandes masas heterogéneas con colecciones líquidas complejas (Figura 6).
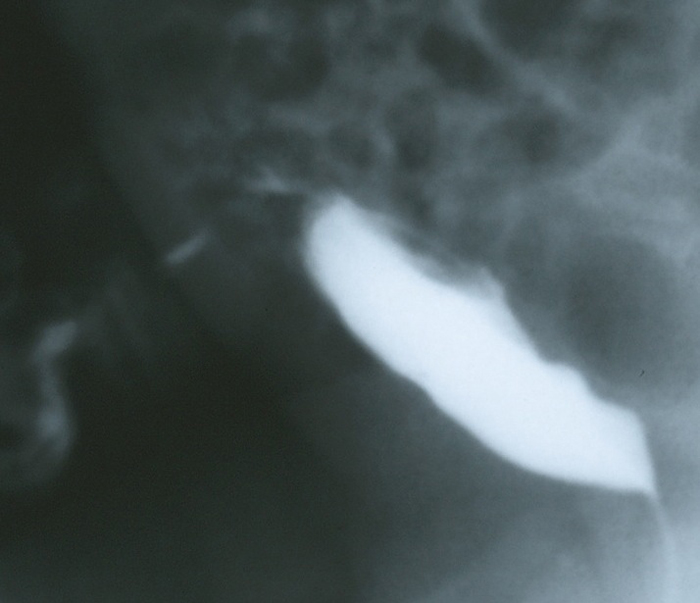
Figura 5 Proyección lateral en fase de llenado de una cistouretrografía miccional (VCUG) en un lactante con grandes cantidades de líquido claro que drena por el ombligo. La imagen demuestra el drenaje de contraste a través de la pared abdominal anterior desde la cúpula vesical por medio de un uraco permeable.
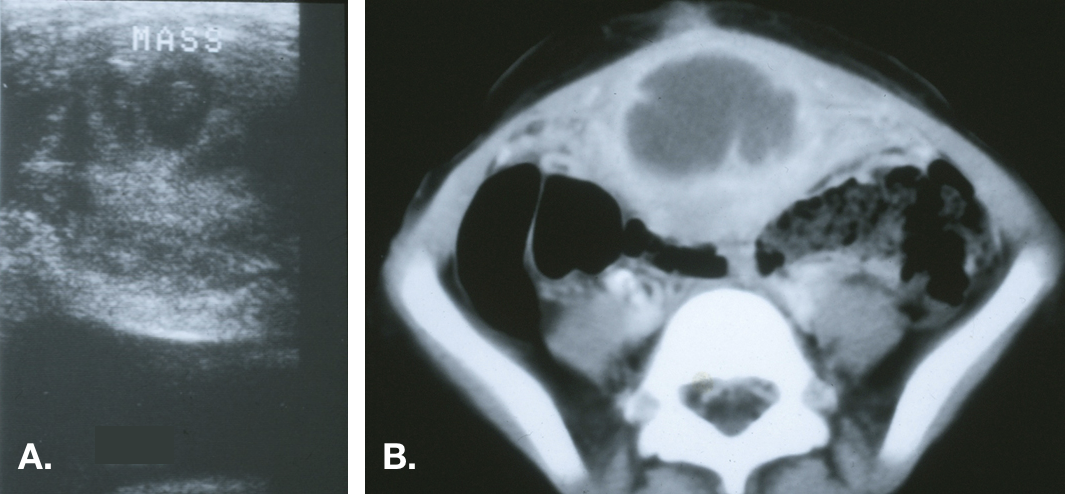
Figura 6 Quiste uracal infectado. A. Vista transversal de la cúpula vesical en la línea media que demuestra una masa ecogénica heterogénea por encima de la vejiga. B. Tomografía computarizada que muestra la masa en la línea media con densidad líquida central, compatible con un absceso, y estriación inflamatoria de la pared abdominal anterior adyacente.
Las lesiones pueden medir varios centímetros de diámetro y, en ocasiones, extenderse más allá del espacio preperitoneal y perforar la cavidad peritoneal.14,15
La TC no debe considerarse un componente integral del estudio diagnóstico de rutina pero puede detectar anomalías pasadas por alto por la ecografía y, por lo tanto, es útil en casos de alta sospecha clínica sin un diagnóstico claro (Figura 7).
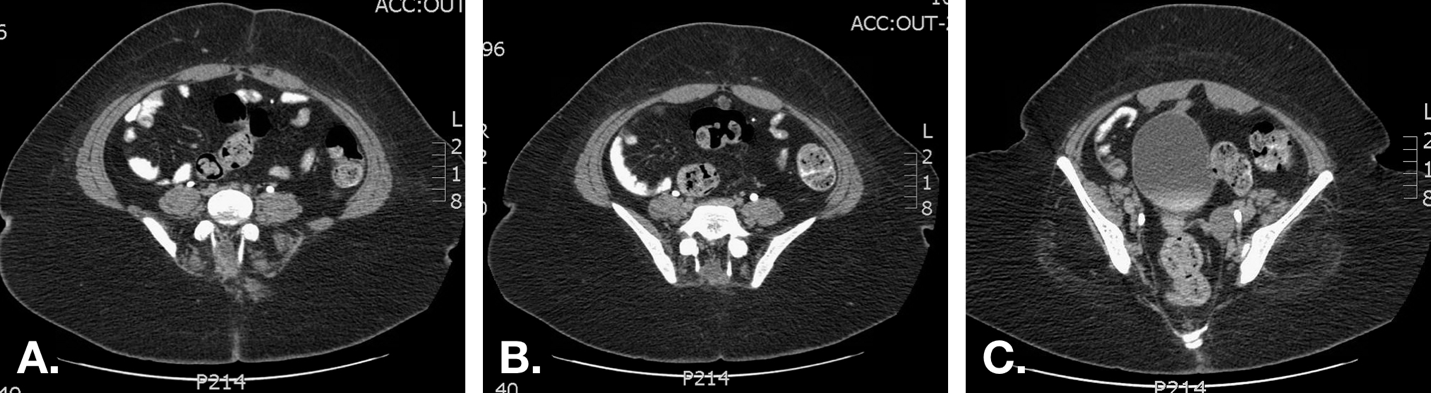
Figura 7 Tomografía computarizada (TC) en un paciente con secreción umbilical sanguinolenta recurrente. A. La imagen justo por debajo del ombligo muestra un uraco de aspecto normal (cordón fibroso) inmediatamente por debajo de los músculos rectos del abdomen en la línea media. B. Se evidencia un quiste uracal más caudalmente. C. Se demuestra la proximidad entre el extremo inferior del quiste y la cúpula vesical.
La evaluación también debe incluir una ecografía renal para asegurar la ausencia de hidronefrosis u otras anomalías renales congénitas.6,8,9,16 La incidencia de anomalías renales concomitantes ha variado ampliamente en las series publicadas, pero, dada la ausencia de morbilidad y riesgo con la ecografía, es prudente incluir estudios de imagen de los riñones como parte de la evaluación diagnóstica.4
Tratamiento
En general, los remanentes uracales sintomáticos deben tratarse con resección quirúrgica. Esto debe incluir la resección completa del uraco desde el ombligo hasta la cúpula vesical (Figura 8).
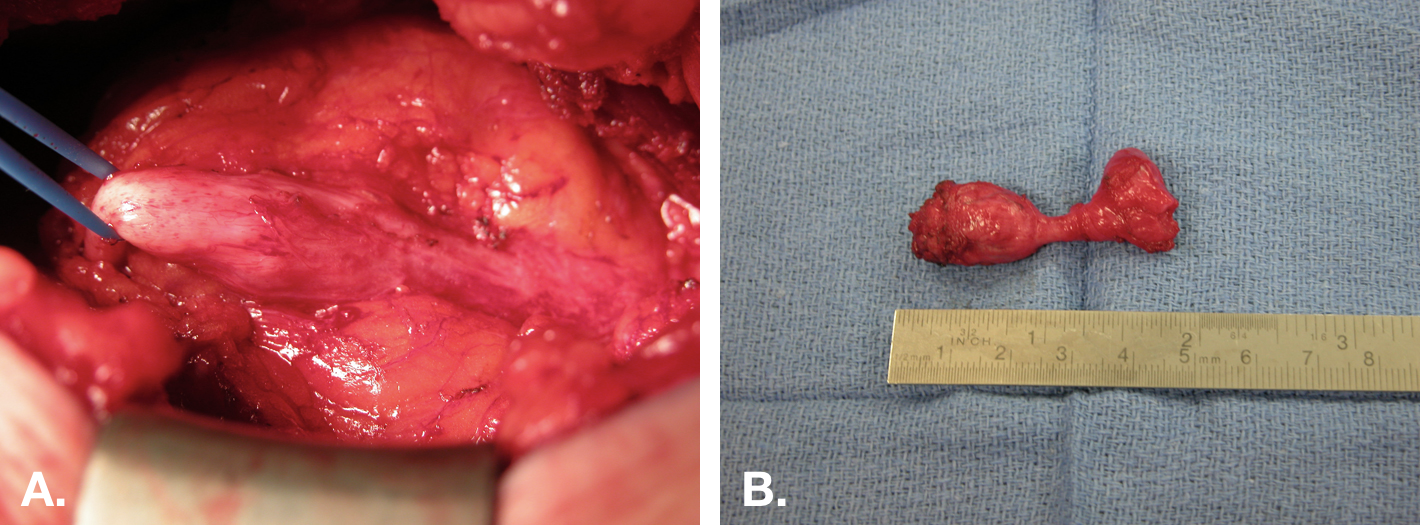
Figura 8 Exéresis abierta de quiste uracal. A. Vista intraoperatoria de la exéresis de un quiste uracal mediante una incisión media infraumbilical. El quiste se encuentra en el centro, con la unión a la vejiga a la derecha, y el cordón fibroso que se extiende hacia el ombligo a la izquierda. B. La pieza (quiste) tras la exéresis con el pequeño manguito de vejiga (extremo derecho de la pieza).
La necesidad de resecar la mucosa vesical en casos de quistes o senos uracales que no están en continuidad con la pared vesical es objeto de debate.2,6,7,17,18 Los quistes uracales infectados plantean otro dilema, ya que el marcado aumento del tamaño del quiste debido a la infección y a la inflamación circundante dificulta la exéresis simple y puede aumentar el riesgo de complicaciones. El quiste uracal infectado puede abordarse en un solo tiempo o en etapas.7,17,19 Los méritos y riesgos relativos de ambos enfoques se analizan más adelante.
La resección quirúrgica del remanente uracal es curativa y no conlleva secuelas funcionales, dado que se trata de un remanente vestigial. El principal dilema quirúrgico se plantea en pacientes que presentan una lesión asintomática descubierta de forma incidental en estudios de imagen.
Manejo conservador
Existen datos limitados sobre las secuelas a largo plazo—a saber, infección recurrente y desarrollo de carcinoma—de las anomalías del uraco dejadas in situ. Históricamente, se favorecía la exéresis dado el riesgo presunto de transformación maligna; sin embargo, publicaciones recientes abogan por un enfoque conservador.10,20 Se han comunicado el cierre del uraco permeable y la regresión de quistes uracales—incluso en el contexto de infección—.21,22,23 La recurrencia de los síntomas tras el drenaje percutáneo de quistes infectados parece ser infrecuente.23 En una serie, el 92% de los lactantes < 6 meses que fueron observados presentó resolución de la infección, mientras que el 60% de quienes se sometieron a exéresis desarrolló una infección posoperatoria, lo que indica que puede ser prudente el manejo conservador hasta al menos los 6 meses de edad.21
En los quistes uracales infectados, se deben obtener un urocultivo y el cultivo del drenaje de la herida, si está presente. El microorganismo aislado con mayor frecuencia en los quistes uracales infectados es Staphylococcus aureus (Tabla 3).5,21,18,20 Si el paciente está estable, afebril, sin aspecto tóxico, sin signos peritoneales, sin celulitis en extensión ni signos de fascitis, puede considerarse el manejo inicial únicamente con antibióticos.
Tabla 3 Especies microbianas cultivadas de restos uracales infectados. * E Coli-3, Citrobacter, Enterococcus y Proteus.
| Autor | # Pacientes | S. Aureus | Estreptococo sp | Otros * |
|---|---|---|---|---|
| Stopak | 16 | 9 | 0 | 2 |
| McCollum | 9 | 6 | 1 | 2 |
| Minevich | 9 | 9 | 0 | 0 |
| Ashley | 9 | 6 | 1 | 2 |
| Galati | 5 | 5 | 0 | 0 |
| Newman | 5 | 3 | 0 | 2 |
| Total | 53 | 38 (72) | 2 (4) | 8 (15) |
En pacientes inestables o en aquellos que no responden al manejo conservador, el quiste infectado puede tratarse mediante escisión quirúrgica completa inicial o drenaje percutáneo (guiado por ecografía o TC) o abierto. En la escisión en un solo tiempo del uraco infectado, los márgenes de resección serán mayores y darán lugar a un defecto de tejidos blandos mayor, y la extensión de la inflamación puede alcanzar la cavidad intraperitoneal, lo que pone en riesgo las vísceras abdominales. Existe un riesgo pequeño pero significativo de fístula enterocutánea y una mayor tasa de complicaciones de la herida tras la escisión primaria de un quiste uracal infectado en comparación con el drenaje.21,18,19,24 Los drenajes percutáneos pueden drenar de forma incompleta colecciones líquidas multiloculadas. Tradicionalmente, todos los quistes se extirpaban tras la resolución de la inflamación en un procedimiento por etapas. Varios estudios recientes han demostrado que la infección recurrente es poco frecuente y, por lo tanto, la escisión diferida puede no ser necesaria.
Resección laparoscópica del uraco
En esta era de la cirugía mínimamente invasiva, han surgido múltiples informes sobre la resección laparoscópica y, más recientemente, laparoscópica asistida por robot de remanentes uracales en niños.25,26,27 También se ha informado la cirugía laparoscópica de puerto único.28 La principal ventaja de la técnica robótica es la facilidad para suturar en comparación con la laparoscopia pura.27 La visualización es excelente con un abordaje laparoscópico para la vejiga, pero puede ser más desafiante a nivel del ombligo si los puertos no se colocan cuidadosamente. El uraco debe resecarse desde la base del ombligo hasta la cúpula de la vejiga. Nuevamente, existe controversia sobre si la resección completa requiere o no la escisión de la cúpula de la vejiga.25,26
La colocación de los puertos es una consideración importante.26 Dado que el uraco se origina en el ombligo, este no puede utilizarse como sitio para un puerto. El sitio más común para la cámara es supraumbilical (por lo general 1–2 cm). Esto proporciona suficiente espacio de trabajo para visualizar la disección desde el ombligo hasta la cúpula vesical. Los puertos de trabajo deben colocarse lateralmente a ambos lados, por lo general a nivel del ombligo. Como alternativa, la colocación lateral de los puertos de trabajo y de la cámara (ya sea en el lado derecho o izquierdo del abdomen) ofrece una visualización lateral del uraco y mantiene todos los puertos en ubicación infraumbilical. La configuración lateral de los puertos hará más difícil suturar el cierre vesical debido al ángulo.

Figura 9 Diagrama de la posible colocación de puertos para la exéresis de un remanente uracal. A diferencia de la configuración habitual en la mayoría de las cirugías laparoscópicas, el ombligo no puede utilizarse como sitio de puerto, ya que es el origen del uraco y debe visualizarse durante la disección.
Exéresis abierta del úraco
En lactantes y niños pequeños, la resección completa del uraco puede lograrse fácilmente a través de una pequeña incisión. Esta puede orientarse ya sea de forma transversal o vertical en la línea media. En los lactantes, una pequeña incisión de 1-1.5 cm a mitad de camino entre el pubis y el ombligo permitirá acceder al uraco y realizar la resección completa desde el ombligo hasta el domo vesical, con excelente exposición del domo vesical para su cierre. Esta pequeña incisión es comparable al tamaño de la incisión necesaria para el puerto de cámara de 12 mm del robot quirúrgico y mantiene el procedimiento enteramente extraperitoneal, eliminando posibles complicaciones intraabdominales. En niños mayores u obesos o en adolescentes, es prudente realizar una incisión vertical en la línea media. Si hay problemas con la exposición, la incisión puede extenderse hacia arriba en dirección al ombligo o hacia abajo hacia la vejiga para facilitar la extirpación completa del uraco en estos pacientes. Las tasas de complicaciones de la escisión simple son muy bajas y la cirugía puede realizarse de forma ambulatoria o con una breve estancia hospitalaria si se deja un catéter colocado. Las fugas de orina o las complicaciones de la herida se asocian con mayor frecuencia a la escisión en un solo tiempo de quistes infectados y no a la escisión simple.18,19
Puntos clave
- Las anomalías del uraco se presentan con mayor frecuencia como secreción umbilical que persiste semanas después del parto o masa umbilical y/o dolor debido a infección.
- El diagnóstico diferencial de la secreción umbilical incluye anomalía del uraco, onfalitis, remanente del conducto onfalomesentérico o un granuloma umbilical.
- Se desconoce el riesgo absoluto de que una anomalía del uraco asintomática desarrolle carcinoma. Los factores de riesgo de carcinoma en una anomalía del uraco incluyen tamaño mayor de 4 cm y edad >55 años.
- La ecografía abdominal es adecuada para el diagnóstico de la anomalía del uraco en la mayoría de los pacientes. La evaluación debe incluir ecografía renal para evaluar anomalías renales congénitas.
- Los remanentes del uraco sintomáticos deben extirparse mediante abordaje abierto, laparoscópico o asistido por robot. Si se utiliza un abordaje laparoscópico o robótico, el ombligo no puede utilizarse como puerto de acceso.
- Las infecciones no complicadas de los quistes del uraco pueden tratarse de forma conservadora con antibióticos ± drenaje percutáneo. La extirpación inmediata conlleva un riesgo significativo de infección posoperatoria. La extirpación diferida es razonable, pero puede no ser necesaria, ya que es posible el cierre de los remanentes/quiste y la infección recurrente es rara, especialmente en niños <6 meses de edad.
Utrículo prostático
Embriología y Anatomía
En los fetos masculinos, la producción de la sustancia inhibidora de Müller (MIS) por las células de Sertoli induce la rápida regresión de los conductos paramesonéfricos (de Müller)—que en las mujeres se convierten en las trompas de Falopio, el oviducto, el útero y los 2/3 superiores de la vagina—en las semanas 8-10ª de gestación. El utrículo prostático es un pequeño remanente de los conductos paramesonéfricos que persiste en los varones como una expansión de la uretra prostática.1 El utrículo se origina en la línea media de la próstata en el aspecto craneal del verumontanum.
Presentación clínica
Los utrículos prostáticos (UP) no son clínicamente significativos a menos que la regresión completa se haya visto comprometida y el utrículo mantenga un aspecto dilatado y quístico, actuando como un divertículo de la uretra prostática. El agrandamiento del utrículo se asocia con hipospadias, criptorquidia, trastornos de la diferenciación sexual y agenesia renal unilateral.29,30,31,32,33,34 Las series de casos indican que la dilatación del UP ocurre en 10-33% de los pacientes con hipospadias proximal, y la incidencia aumenta con la gravedad del defecto de hipospadias.30,32 En una serie de niños con genitales externos normales y UP sintomático, se encontró agenesia renal unilateral en casi un tercio de los casos.33
PU puede ser asintomático, causar síntomas relacionados con obstrucción o estasis urinaria—infecciones del tracto urinario recurrentes, epididimo-orquitis, secreción uretral, retención, formación de cálculos o goteo posmiccional—o puede presentarse con dolor abdominal, hematuria o hemospermia.31,33,35 En raras ocasiones, se ha informado transformación maligna.33,34,36
La dilatación del utrículo prostático puede dificultar la cateterización de varones con hipospadias—la dificultad para la cateterización puede ser la forma de presentación o el único síntoma del utrículo prostático en estos pacientes. Los utrículos grandes pueden ser palpables por debajo o por detrás de la vejiga en el examen rectal digital.31,33,35,37
El diagnóstico diferencial de los utrículos prostáticos incluye el quiste del conducto de Müller (no está en continuidad con la uretra prostática), el divertículo vesical, el quiste uracal y el quiste de la vesícula seminal.33,38
Tabla 4 Síntomas de presentación de los pacientes con utrículos prostáticos
| Autor | # Pacientes | ITU | STUI | Retención | Epididimitis/ Dolor escrotal | Otros |
|---|---|---|---|---|---|---|
| Desautel | 26 | 6 | 1 | 7 | 2 | 1 |
| Liu | 22 | 8 | 7 | 6 | 3 | 6 |
| Dai | 15 | 6 | 2 | 1 | 7 | 4 |
| Jia | 14 | 8 | 1 | 1 | 5 | 3 |
| Babu | 7 | 3 | 2 | 1 | 3 | 1 |
| Total | 84 | 31 (37) | 13 (15) | 16 (19) | 20 (24) | 5 (6) |
Evaluación radiológica
El diagnóstico a menudo se establece mediante uretrografía retrógrada (RUG) o cistouretrografía miccional (VCUG) ya que estas modalidades permiten la visualización del orificio del utrículo en relación con la uretra y la vejiga. Sin embargo, la ecografía transabdominal es casi tan sensible como el RUG y puede ser adecuada para detectar utrículos lo suficientemente grandes como para justificar una intervención.30,39 Los utrículos pueden pasarse por alto en las imágenes debido a un llenado incompleto. Pueden realizarse estudios de imagen de corte transversal que pueden ayudar en la planificación quirúrgica, pero no son necesarios para el diagnóstico. Los utrículos pueden clasificarse en las imágenes de la siguiente manera:29
- Grado 0 – confinado al verumontanum
- Grado 1 – se extiende hasta o por debajo del cuello vesical (Imagen 1)
- Grado 2 – se extiende proximal al cuello vesical (Imagen 2)
- Grado 3 – se abre distal al esfínter uretral externo
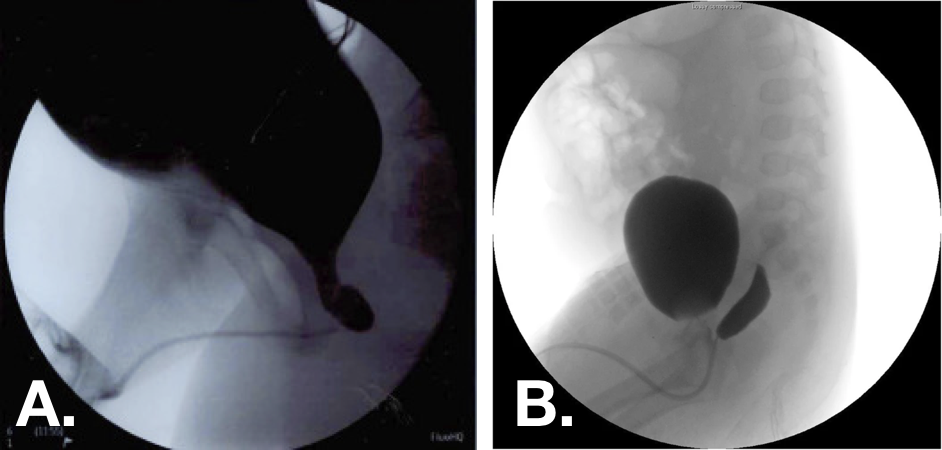
Figura 10 Imágenes de cistouretrografía miccional (VCUG) que muestran utrículos prostáticos de grado 1 (izquierda) y de grado 2 (derecha).30,33
Manejo
El manejo conservador exitoso de los utrículos sintomáticos no ha sido bien descrito y, por lo general, requeriría profilaxis antibiótica frecuente o a largo plazo para infecciones recurrentes.33 Se ha descrito una variedad de abordajes quirúrgicos exitosos, siendo la exéresis completa del utrículo el tratamiento definitivo. Para utrículos con orificios muy pequeños, se han reportado la aspiración guiada por ecografía transrectal y la cateterización y aspiración transuretral, la incisión del orificio y la fulguración.31,33,35,40 Estos abordajes son mínimamente invasivos, pero conllevan una mayor incidencia de recurrencia de los síntomas que la exéresis. Se han descrito abordajes abiertos, laparoscópicos y asistidos por robot para la exéresis, y no existe consenso respecto al abordaje óptimo. El abordaje robótico puede ser ventajoso debido a la localización difícil del utrículo. Se puede acceder a los utrículos mediante abordajes extraperitoneales, extravesicales, transvesicales, sagitales posteriores o perineales.31,33,35,37,41 La cistoscopia concomitante puede ayudar a definir los límites de la disección en procedimientos laparoscópicos.37,41 Las conversiones descritas de abordajes laparoscópicos a abiertos para la exéresis del utrículo son poco frecuentes.
Los principios clave de la escisión, independientemente del abordaje, son una disección adecuada, la escisión y el cierre hermético del orificio del utrículo, y la evitación de lesiones de los nervios pélvicos, del conducto deferente, de los vasos seminales, de los colículos seminales y del recto.
Tabla 5 Enfoques quirúrgicos para la exéresis del utrículo prostático y recurrencia posoperatoria de los síntomas de presentación
| Enfoque | Endoscópico | Endoscópico | Abierto | Abierto | Laparoscópico | Laparoscópico |
|---|---|---|---|---|---|---|
| Autor | Casos | Recurrencia | Casos | Recurrencia | Casos | Recurrencia |
| Liu | 3 | 0 | 11 | 0 | 4 | 0 |
| Desautel | 2 | 1 | 13 | 0 | – | – |
| Dai | 13 | 5 | – | – | 4 | 0 |
| Jia | – | – | 8 | 2 | 6 | 0 |
| Babu | 7 | 2 | 2 | 2 | 1 | 1 |
| Yeung | – | – | – | – | 4 | 0 |
| Bayne | – | – | – | – | 4 | 0 |
| Total | 25 | 8 (32) | 34 | 4 (12) | 23 | 1 (4) |
Puntos clave
- El utrículo prostático es un pequeño remanente de los conductos paramesonéfricos que persiste en los varones como una expansión de la uretra prostática.
- El agrandamiento del utrículo se asocia con hipospadias, criptorquidia, trastornos de la diferenciación sexual y agenesia renal unilateral.
- Los utrículos prostáticos pueden ser asintomáticos, causar síntomas relacionados con obstrucción o estasis urinaria, o presentarse con dolor abdominal, hematuria o hematospermia.
- La dilatación del utrículo prostático puede dificultar la cateterización de varones con hipospadias.
- Los utrículos prostáticos sintomáticos pueden extirparse mediante abordaje abierto, laparoscópico o asistido por robot.
Divertículos vesicales
Los divertículos vesicales son poco frecuentes en la población pediátrica, presentándose en el 1,7 % de los pacientes.42 Los divertículos pueden ser congénitos o adquiridos; los divertículos vesicales congénitos son mucho más frecuentes en la población pediátrica.43
Divertículos congénitos
Los divertículos congénitos se consideran el resultado de un defecto del músculo detrusor. El noventa por ciento se desarrollan alrededor de la vaina de Waldeyer, que contiene el uréter, y se conocen como divertículos de Hutch.44 Pueden clasificarse como periureterales (divertículo cercano pero que no compromete el orificio ureteral) o paraureterales (el orificio ureteral está involucrado en el divertículo).44 La distorsión de la pared vesical y del túnel muscular del uréter predispone a los niños con estos divertículos al reflujo vesicoureteral. Los divertículos congénitos no asociados con el uréter se desarrollan en la pared vesical posterolateral.43
Los divertículos vesicales congénitos están asociados con síndromes genéticos que afectan el desarrollo del tejido conectivo: Ehlers-Danlos tipos IV, V, IX; síndrome de Menkes; síndrome de Williams-Beuren y síndrome alcohólico fetal.41,44,45 A diferencia de los divertículos adquiridos, los divertículos congénitos se encuentran en vejigas de pared lisa que típicamente presentan una mecánica miccional normal, son defectos solitarios y no se asocian con un mayor riesgo de malignidad.43 Los divertículos congénitos ocurren con mayor frecuencia en varones y generalmente son más grandes que los adquiridos por disfunción vesical neurógena.43
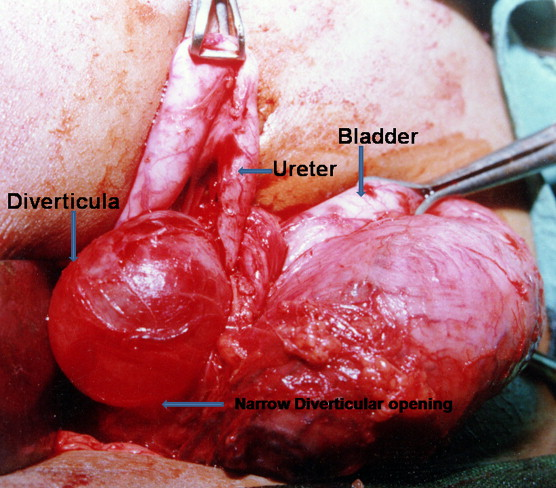
Figura 11 Demostración intraoperatoria de un gran divertículo vesical paraureteral con dilatación proximal y desplazamiento medial del uréter.46
Divertículos adquiridos
Los divertículos adquiridos o secundarios se desarrollan debido a patología neurogénica u obstructiva en el tracto urinario inferior. Aunque son el tipo de divertículo más común en adultos, los divertículos secundarios son raros en pacientes pediátricos e indican una disfunción grave del tracto urinario inferior.43 Es más probable encontrarlos cerca de la cúpula vesical, pueden ser múltiples y es más probable observarlos en una vejiga trabeculada. En general, los divertículos adquiridos se asocian con vejiga neurógena y obstrucción de la salida vesical, y en pacientes pediátricos pueden observarse con válvulas uretrales posteriores & síndrome de abdomen en ciruela pasa.42,43
Presentación clínica
Los divertículos vesicales en niños se presentan con mayor frecuencia con ITU secundaria a estasis urinaria dentro del divertículo o se descubren durante el estudio de hidronefrosis o de una ITU febril y sospecha de reflujo vesicoureteral.44,46 Se pueden encontrar anomalías del tracto urinario superior en 16-30% de los casos.44 Los síntomas de presentación menos frecuentes incluyen síntomas miccionales irritativos, hematuria, distensión y dolor abdominal, enuresis, litiasis vesical y obstrucción de la salida vesical por distorsión del cuello vesical.46,47,48 En raras ocasiones, los divertículos vesicales pueden presentarse con obstrucción ureteral completa o perforación intra- o extraperitoneal.49,50,51,52,53,54
La mayoría de los pacientes con divertículos vesicales congénitos son asintomáticos y—aunque con mucha menor frecuencia que los divertículos adquiridos—pueden ser diagnosticados incidentalmente en adultos.
Dada la asociación con diversas afecciones genéticas, la frecuencia de anomalías del tracto urinario superior y la posibilidad de una enfermedad subyacente neurogénica u obstructiva, algunos han propuesto que a todos los niños con divertículos vesicales se les realicen pruebas para detectar anomalías cromosómicas.42 En la actualidad no se recomienda realizar pruebas genéticas de rutina en pacientes con divertículo vesical congénito único.44
Tabla 6 Síntomas de presentación y hallazgos asociados en niños con divertículos vesicales
| Autores | # Pacientes | ITU | STUI | Retención | Otros | RVU | Hidronefrosis |
|---|---|---|---|---|---|---|---|
| Alexander | 47 | 26 | 2 | 0 | 2 | 32 | 19 |
| Evangilidis | 21 | 19 | 12 | 0 | – | – | – |
| Marte | 16 | 15 | 9 | 0 | 6 | 7 | – |
| Bhat | 12 | 5 | – | 12 | 4 | 9 | 5 |
| Macedo | 10 | 5 | 3 | 1 | – | – | 4 |
| Total | 106 | 70 (66) | 26 (25) | 13 (12) | 12 (11) | 48 (45) | 28 (26) |
Evaluación radiológica
Los divertículos vesicales a menudo se detectan por primera vez en la ecografía vesical como un quiste hipoecoico que se proyecta desde la pared vesical posterolateral. El diagnóstico diferencial de un divertículo sospechado en los estudios de imagen incluye quiste uracal, ureterocele evertido, uréter ectópico, herniación vesical en hernia inguinal y duplicación vesical.44 La cistouretrografía miccional con proyecciones laterales y oblicuas es el estándar de oro para establecer el diagnóstico de divertículo vesical y permite la evaluación simultánea del VUR.43 En particular, en los casos sin VUR, el pielograma intravenoso o el urograma por TC o RM pueden utilizarse para aclarar la relación anatómica entre el divertículo y el uréter.44 Las vías urinarias superiores de los niños con divertículos vesicales deben evaluarse para hidroureteronefrosis.
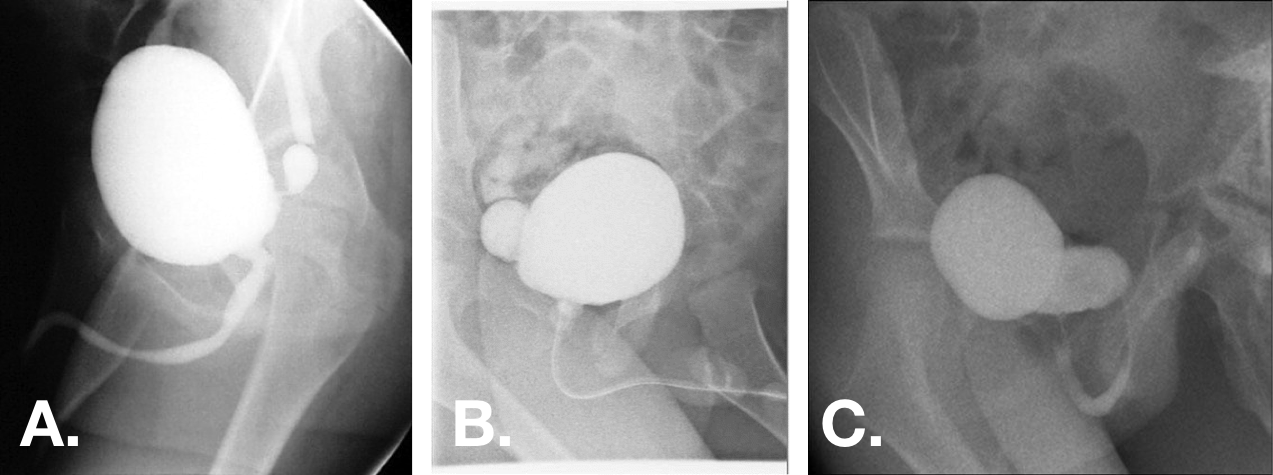
Figura 12 Divertículos vesicales congénitos observados en vistas oblicuas de VCUG. Los divertículos pueden variar desde pequeños con cuellos muy estrechos hasta más grandes que la vejiga, con orificios de base amplia.44,47,55
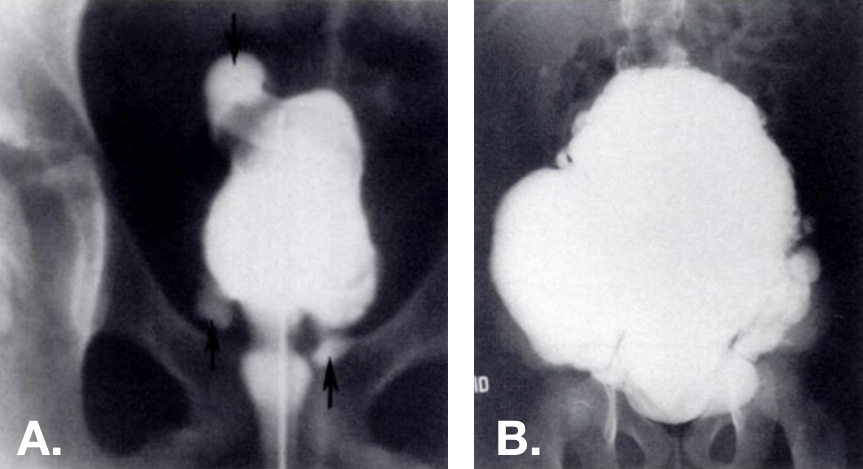
Figura 13 Divertículos adquiridos observados en la VCUG. Múltiples divertículos presentes en varias localizaciones—incluida la cúpula vesical—en vejigas trabeculadas. La foto de la derecha es de un paciente con síndrome de Ehlers-Danlos.42
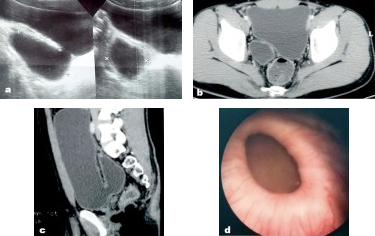
Figura 14 Divertículo vesical congénito observado en la ecografía, la TC pélvica y la cistoscopia.56
Los estudios urodinámicos pueden considerarse en pacientes con divertículos vesicales si se sospecha disfunción del tracto urinario inferior subyacente o si la presencia de un divertículo no explica adecuadamente los síntomas de presentación del paciente. La hiperactividad del detrusor puede observarse en alrededor de la mitad de estos pacientes, posiblemente secundaria a hipotonía dentro y alrededor del divertículo y a estasis urinaria crónica.44,48 Los divertículos complican la interpretación del cistometrograma, ya que disminuyen la presión intravesical. La estasis de orina dentro del divertículo y el RVU asociado también pueden complicar los resultados.44
La evaluación endoscópica puede ayudar a aclarar la anatomía y se recomienda durante la intervención quirúrgica, pero no es necesaria para el diagnóstico del divertículo vesical.
Indicaciones para la reparación
Aunque los divertículos vesicales no se resuelven sin intervención, no todos los pacientes requieren cirugía. El tratamiento adecuado de la infección del tracto urinario (ITU) y de la disfunción miccional puede resolver los síntomas en pacientes con divertículos pequeños y no complicados.44 Para aquellos con síntomas refractarios o divertículos complicados, la exéresis quirúrgica suele ser curativa, y puede realizarse simultáneamente la reimplantación ureteral según sea necesario. Las indicaciones generalmente aceptadas para cirugía incluyen las siguientes:43,44
- Síntomas miccionales refractarios al manejo médico
- Divertículo > 3cm
- ITU frecuentes
- RVU complicado
- Retención urinaria
- Obstrucción o deterioro de la vía urinaria superior
- Litiasis vesical
- Rotura de divertículo
A diferencia de los adultos, la degeneración maligna del epitelio asociada con divertículos vesicales pediátricos generalmente no se observa; sin embargo, cualquier sospecha de malignidad requeriría una intervención quirúrgica.43
Antes de cualquier intervención quirúrgica, la disfunción miccional debe ser evaluada y tratada con el fin de aislar los síntomas relacionados con el divertículo y su evolución posoperatoria. La patología asociada, como la hipocontractilidad del detrusor, la obstrucción del tracto de salida vesical o el disrafismo espinal, debe abordarse antes de la diverticulectomía.
La intervención quirúrgica debe considerarse cuidadosamente en pacientes con trastornos subyacentes del tejido conectivo, ya que la recurrencia es probable en esta población.44,53
Abordajes quirúrgicos
La diverticulectomía vesical puede realizarse endoscópicamente o mediante abordajes abiertos o mínimamente invasivos transvesicales o extravesicales. Los abordajes transvesicales y extravesicales replican los utilizados para la reimplantación ureteral, y la reimplantación puede realizarse como parte del procedimiento si es necesario debido a la localización del divertículo o si está indicada por reflujo vesicoureteral (RVU) asociado grave. Se recomienda la evaluación cistoscópica del orificio diverticular respecto al orificio ureteral como parte de la planificación quirúrgica. Varias series de casos han comunicado la resolución completa de los síntomas—o una reducción marcada de los síntomas de disfunción miccional—así como del RVU tras la exéresis del divertículo independientemente del abordaje.57,55 Se ha comunicado la oclusión del orificio diverticular paraureteral mediante inyección subureteral de agentes de relleno, aunque los datos sobre la eficacia a largo plazo son limitados.58,59 Una comparación de los abordajes endoscópico, intravesical y extravesical demostró la resolución exitosa del RVU en el 79, 91 y 80% de los casos, respectivamente.59
Las consideraciones quirúrgicas importantes, independientemente del abordaje, son la profilaxis antimicrobiana perioperatoria guiada por cultivo, la prevención de lesión o desvascularización del uréter o del conducto deferente, la prevención de lesión rectal en la reparación de divertículos posteriores grandes y la descompresión vesical posoperatoria.44
Puntos clave
- Los divertículos vesicales en niños pueden ser congénitos—debido a un defecto del músculo detrusor, con mayor frecuencia alrededor de la vaina de Waldeyer (divertículos de Hutch)—o adquiridos debido a patología neurogénica u obstructiva del tracto urinario inferior.
- La distorsión de la pared vesical y del túnel muscular del uréter por los divertículos de Hutch predispone a los niños al reflujo vesicoureteral.
- Los divertículos vesicales en niños se presentan con mayor frecuencia con ITU secundaria a estasis urinaria dentro del divertículo o se descubren durante la evaluación de hidronefrosis o de ITU febril y sospecha de reflujo vesicoureteral. La mayoría de los divertículos son asintomáticos.
- El cistouretrograma miccional con proyecciones laterales y oblicuas es el estándar de oro para establecer el diagnóstico de divertículo vesical y permite la evaluación simultánea del RVU.
- Para aquellos con síntomas refractarios o divertículos complicados, puede realizarse la exéresis quirúrgica mediante abordaje transvesical o extravesical. La reimplantación ureteral puede realizarse simultáneamente según sea necesario.
- Antes de cualquier intervención quirúrgica, debe evaluarse y tratarse la disfunción miccional.
Resumen
Las anomalías del uraco pueden presentarse de diversas formas y con mayor frecuencia ocasionan drenaje desde el ombligo o infección. Las anomalías pueden manejarse de forma conservadora y pueden resolverse espontáneamente. Los quistes infectados pueden drenarse de forma percutánea, y cualquier anomalía sintomática puede extirparse mediante abordajes abiertos o laparoscópicos. Se desconoce el riesgo de transformación maligna de las anomalías uracales asintomáticas en niños.
La dilatación del utrículo prostático se asocia con hipospadias y otras anomalías genitourinarias, y puede ser asintomática o causar síntomas relacionados con obstrucción de la salida y estasis urinaria. Los utrículos pueden diagnosticarse mediante RUG, VCUG o US. En pacientes sintomáticos, la extirpación puede realizarse por abordajes endoscópico, abierto o laparoscópico, siendo el manejo endoscópico el que confiere un mayor riesgo de recurrencia.
Los divertículos vesicales pediátricos pueden ser congénitos o adquiridos. Los divertículos congénitos se deben a defectos del detrusor cerca de la vaina del uréter y se asocian con RVU, así como con trastornos del tejido conectivo. Los divertículos son con frecuencia asintomáticos, pero pueden causar infección, síntomas miccionales irritativos, retención urinaria o dolor abdominal y a menudo se asocian con hiperactividad del detrusor. Los divertículos adquiridos son secundarios a obstrucción del tracto urinario inferior o a vejiga neurógena. Las indicaciones para la reparación quirúrgica incluyen síntomas refractarios o graves, tamaño >3cm y disfunción asociada del tracto urinario. La intervención debe estar precedida por el manejo de cualquier otra patología del tracto urinario inferior. No hay consenso respecto al abordaje quirúrgico, y el reimplante ureteral a menudo se realiza de manera simultánea.
Referencias
- Jm P. Embryology of the genitourinary tract. Elsevier: Philadelphia; 2016, DOI: 10.1201/b13795-15.
- MacNeily AE, Koleilat N, Kiruluta HG, Homsy YL. Urachal abscesses: Protean manifestations, their recognition, and management. Urology 1992; 40 (6): 530–535. DOI: 10.1016/0090-4295(92)90409-p.
- Naiditch JA, Radhakrishnan J, Chin AC. Current diagnosis and management of urachal remnants. J Pediatr Surg 2013; 48 (10): 2148–2152. DOI: 10.1016/j.jpedsurg.2013.02.069.
- Fox JA, M.S. R, JC G, CF A, RA H, JC V, et al.. Vesicoureteral reflux in children with urachal anomalies. J Pediatr Urol 2011; 7 (6): 632–635. DOI: 10.1016/j.jpurol.2011.04.001.
- Ashley RA, Inman BA, Routh JC, Rohlinger AL, Husmann DA, Kramer SA. Urachal Anomalies: A Longitudinal Study of Urachal Remnants in Children and Adults. J Urol 2007; 178 (4s): 1615–1618. DOI: 10.1016/j.juro.2007.03.194.
- Cilento BG, Bauer SB, Retik AB, Peters CA, Atala A. Urachal anomalies: defining the best diagnostic modality. Urology 1998; 52 (1): 120–122. DOI: 10.1016/s0090-4295(98)00161-7.
- Rich RH, Hardy BE, Filler RM. Surgery for Anomalies of the Urachus. J Urol 1983; 131 (3): 616–616. DOI: 10.1016/s0022-5347(17)50535-2.
- Yiee JH, Garcia N, Baker LA, Barber R, Snodgrass WT, Wilcox DT. A diagnostic algorithm for urachal anomalies. J Pediatr Urol 2007; 3 (6): 500–504. DOI: 10.1016/j.jpurol.2007.07.010.
- Copp HL, Wong IY, Krishnan C, Malhotra S, Kennedy WA. Clinical Presentation and Urachal Remnant Pathology: Implications for Treatment. J Urol 2009; 182 (4s): 1921–1924. DOI: 10.1016/j.juro.2009.03.026.
- Cuda SP, Vanasupa BP, Sutherland RS. Nonoperative management of a patent urachus. Urology 2005; 66 (6): 1320.e7–1320.e9. DOI: 10.1016/j.urology.2005.06.121.
- Gleason JM, Bowlin PR, Bagli DJ, Lorenzo AJ, Hassouna T, Koyle MA, et al.. A Comprehensive Review of Pediatric Urachal Anomalies and Predictive Analysis for Adult Urachal Adenocarcinoma. J Urol 2015; 193 (2): 632–636. DOI: 10.1016/j.juro.2014.09.004.
- Stopak JK, Azarow KS, Abdessalam SF, Raynor SC, Perry DA, Cusick RA. Trends in surgical management of urachal anomalies. J Pediatr Surg 2015; 50 (8): 1334–1337. DOI: 10.1016/j.jpedsurg.2015.04.020.
- Dethlefs CR, Abdessalam SF, Raynor SC, Perry DA, Allbery SM, Lyden ER, et al.. Conservative management of urachal anomalies. J Pediatr Surg 2019; 54 (5): 1054–1058. DOI: 10.1016/j.jpedsurg.2019.01.039.
- Sheldon CA, Clayman RV, Gonzalez R, Williams RD, Fraley EE. Malignant Urachal Lesions. J Urol 1984; 131 (1): 1–8. DOI: 10.1016/s0022-5347(17)50167-6.
- Oestreich AE. Urachal anomalies in children: the vanishing relevance of the preoperative voiding cystourethrogram. Yearbook of Diagnostic Radiology 2005; 2007 (12): 174–175. DOI: 10.1016/s0098-1672(08)70123-1.
- Lewis JB, Morse JW, Eyolfson MF, Schwartz SL. Spontaneous Rupture of a Vesicourachal Diverticulum Manifesting as Acute Abdominal Pain. Acad Emerg Med 1996; 3 (12): 1140–1143. DOI: 10.1111/j.1553-2712.1996.tb03375.x.
- OGBEVOEN JUSTINO, JAFFE DAVIDM, LANGER JACOBC. Intraperitoneal rupture of an infected urachal cyst: A rare cause of peritonitis in children. Pediatr Emerg Care 1996; 12 (1): 41–43. DOI: 10.1097/00006565-199602000-00012.
- GONZ??LEZ RICARDO, De FILIPPO ROGER, JEDNAK ROMAN, BARTHOLD JULIASPENCER. Urethral Atresia: Long-term Outcome In 6 Children Who Survived The Neonatal Period. J Urol 2001: 2241–2244. DOI: 10.1097/00005392-200106001-00006.
- Mesrobian H-GO, Zacharias A, Balcom AH, Cohen RD. Ten Years of Experience With Isolated Urachal Anomalies in Children. J Urol 1997; 158: 1316–1318. DOI: 10.1097/00005392-199709000-00173.
- McCollum MO, MacNeily AE, Blair GK. Surgical implications of urachal remnants: Presentation and management. J Pediatr Surg 2003; 38 (5): 798–803. DOI: 10.1016/jpsu.2003.50170.
- Minevich E, W.J. L, A.G.. The infected urachal cyst: Primary excision versus a staged approach. J Pediatr Surg 1997; 33 (1): 147. DOI: 10.1016/s0022-3468(98)90408-0.
- Newman BM, Karp MP, Jewett TC, Cooney DR. Advances in the management of infected urachal cysts. J Pediatr Surg 1986; 21 (12): 1051–1054. DOI: 10.1016/0022-3468(86)90006-0.
- Yoo KH, Lee S-J, Chang S-G. Treatment of Infected Urachal Cysts. Yonsei Med J 2006; 47 (3): 423. DOI: 10.3349/ymj.2006.47.3.423.
- Galati VG, D.B. R, F.. Management of Urachal Remnants in Early Childhood. Yearbook of Diagnostic Radiology 2008; 2009: 154–155. DOI: 10.1016/s0098-1672(09)79312-9.
- Nogueras-Ocaña M, Rodríguez-Belmonte R, Uberos-Fernández J, Jiménez-Pacheco A, Merino-Salas S, Zuluaga-Gómez A. Urachal anomalies in children: Surgical or conservative treatment? J Pediatr Urol 2014; 10 (3): 522–526. DOI: 10.1016/j.jpurol.2013.11.010.
- Lipskar AM, Glick RD, Rosen NG, Layliev J, Hong AR, Dolgin SE, et al.. Nonoperative management of symptomatic urachal anomalies. J Pediatr Surg 2010; 45 (5): 1016–1019. DOI: 10.1016/j.jpedsurg.2010.02.031.
- Stone NM, Garden RJ, Webert H. Laparoscopic excision of a urachal cyst. Urology 1995; 45 (1): 161–164. DOI: 10.1016/s0090-4295(95)97824-0.
- OKEGAWA TAKATSUGU, ODAGANE AKIHIRO, NUTAHARA KIKUO, HIGASHIHARA EIJI. Laparoscopic management of urachal remnants in adulthood. Int J Urol 2005; 13 (12): 1466–1469. DOI: 10.1111/j.1442-2042.2006.01613.x.
- Yamzon J, K.P. DF, RE C, AY H, BE K, C.J.. V1710 Pediatric Robotic-assisted Laparoscopic Urachal Cyst And Bladder Cuff Excision. J Urol 2008; 185 (4s): 2385–2388. DOI: 10.1016/j.juro.2011.02.2035.
- Patrzyk M, Glitsch A, Schreiber A, Bernstorff W von, Heidecke C-D. Single-incision laparoscopic surgery as an option for the laparoscopic resection of an urachal fistula: first description of the surgical technique. Surg Endosc 2010; 24 (9): 2339–2342. DOI: 10.1007/s00464-010-0922-4.
- IKOMA F, SHIMA H, YABUMOTO H. Classification of Enlarged Prostatic Utricle in Patients with Hypospadias. Br J Urol 1985; 57 (3): 334–337. DOI: 10.1111/j.1464-410x.1985.tb06356.x.
- Aktuğ T, Ekberli\. G. Re: The prostatic utricle: an under-recognized condition resulting in significant morbidity in boys with both hypospadias and normal external genitalia. J Pediatr Urol 2017; 15 (4): 425. DOI: 10.1016/j.jpurol.2019.03.030.
- Dai L-N, He R, Wu S-F, Zhao H-T, Sun J. Surgical treatment for prostatic utricle cyst in children: A single-center report of 15 patients. Int J Urol 2021; 28 (6): 689–694. DOI: 10.1111/iju.14543.
- Devine CJ, Gonzalez-Serva L, Stecker JF, Devine PC, Horton CE. Utricular Configuration in Hypospadias and Intersex. J Urol 1980; 123 (3): 407–411. DOI: 10.1016/s0022-5347(17)55959-5.
- Liu B, He D, Zhang D, Liu X, Lin T, Wei G. Prostatic utricles without external genital anomalies in children: our experience, literature review, and pooling analysis. BMC Urol 2019; 19 (1): 21. DOI: 10.1186/s12894-019-0450-z.
- Farikullah J, Ehtisham S, Nappo S, Patel L, Hennayake S. Persistent Müllerian duct syndrome: lessons learned from managing a series of eight patients over a 10-year period and review of literature regarding malignant risk from the Müllerian remnants. BJU Int 2012; 110 (11c): E1084–e1089. DOI: 10.1111/j.1464-410x.2012.11184.x.
- Desautel MG, Stock J, Hanna MK, REMNANTS MULLERIANDUCT. Müllerian Duct Remnants. J Urol 1999; 162 (3, Part 2): 1014. DOI: 10.1097/00005392-199909000-00013.
- Jia W, L.G. Z, L W, Y F, W H, J X, et al.. Comparison of laparoscopic excision versus open transvesical excision for symptomatic prostatic utricle in children J Pediatr Surg. 2016; 51 (10): 1597–1601. DOI: 10.1016/j.jpedsurg.2016.06.004.
- Babu R, Chandrasekharam VVS. Cystoscopic Management of Prostatic Utricles. Urology 2021; 149: e52–e55. DOI: 10.1016/j.urology.2020.09.005.
- Nallabothula AK, Yatam LS, Ayapati T, Bodagala VD. Large Prostatic Utricle With Transitional Cell Carcinoma in an Adult. Urology 2017; 102: e5–e6. DOI: 10.1016/j.urology.2016.12.048.
- Yeung CK, Sihoe JDY, Tam YH, Lee KH. Laparoscopic excision of prostatic utricles in children. BJU Int 2001; 87 (6): 505–508. DOI: 10.1046/j.1464-410x.2001.00132.x.
- Johnson D, Parikh K, Schey W, Mar W. MRI in Diagnosis of a Giant Prostatic Utricle. Case Rep Radiol 2014; 2014: 1–3. DOI: 10.1155/2014/217563.
- Kojima Y, Hayashi Y, Maruyama T, Sasaki S, Kohri K. Comparison between ultrasonography and retrograde urethrography for detection of prostatic utricle associated with hypospadias. Urology 2001; 57 (6): 1151–1155. DOI: 10.1016/s0090-4295(01)00954-2.
- Bayne AP, Austin JC, Seideman CA. Robotic assisted retrovesical approach to prostatic utricle excision and other complex pelvic pathology in children is safe and feasible. J Pediatr Urol 2021; 17 (5): 710–715. DOI: 10.1016/j.jpurol.2021.08.004.
- Blane CE, Zerin JM, Bloom DA. Bladder diverticula in children. Radiology 1994; 190 (3): 695–697. DOI: 10.1148/radiology.190.3.8115613.
- Es R. Bladder and female urethral diverticula. Elsevier: Philadelphia; 2017, DOI: 10.1016/b978-1-4160-6911-9.00078-5.
- Psutka SP, Cendron M. Bladder diverticula in children. J Pediatr Urol 2013; 9 (2): 129–138. DOI: 10.1016/j.jpurol.2012.02.013.
- Sammour Z, Gomes C, Bessa J, Pinheiro M, Kim C, Sacomani C, et al.. 1622 Congenital Genitourinary Abnormalities In Children With Williams-beuren Syndrome. J Urol 2014; 187 (4s): 804–809. DOI: 10.1016/j.juro.2012.02.1417.
- Bhat A, Bothra R, Bhat MP, Chaudhary GR, Saran RK, Saxena G. Congenital bladder diverticulum presenting as bladder outlet obstruction in infants and children. J Pediatr Urol 2012; 8 (4): 348–353. DOI: 10.1016/j.jpurol.2011.07.001.
- Alexander RE, Kum JB, Idrees M. Bladder Diverticulum: Clinicopathologic Spectrum in Pediatric Patients. Pediatr Dev Pathol 2012; 15 (4): 281–285. DOI: 10.2350/12-02-1154-oa.1.
- Evangelidis A, Castle EP, Ostlie DJ, Snyder CL, Gatti JM, Murphy JP. Surgical management of primary bladder diverticula in children. J Pediatr Surg 2005; 40 (4): 701–703. DOI: 10.1016/j.jpedsurg.2005.01.003.
- Marte A, Cavaiuolo S, Esposito M, Pintozzi L. Vesicoscopic Treatment of Symptomatic Congenital Bladder Diverticula in Children: A 7-Year Experience. Eur J Pediatr Surg 2015; 26 (03): 240–244. DOI: 10.1055/s-0035-1551564.
- Cruz ML da, Macedo A, Garrone G, Ottoni SL, Oliveira DE, Rosário Souza GRM do. Primary congenital bladder diverticula: Where does the ureter drain? Afr J Paediatr Surg 2015; 12 (4): 280. DOI: 10.4103/0189-6725.172574.
- Livne PM, Gonzales ET. Congenital bladder diverticula causing ureteral obstruction. Urology 1985; 25 (3): 273–276. DOI: 10.1016/0090-4295(85)90327-9.
- Stein RJ, Matoka DJ, Noh PH, Docimo SG. Spontaneous perforation of congenital bladder diverticulum. Urology 2005; 66 (4): 881.e5–881.e6. DOI: 10.1016/j.urology.2005.04.004.
- Britto MM, Yao HHI, Campbell N. Delayed diagnosis of spontaneous rupture of a congenital bladder diverticulum as a rare cause of an acute abdomen. ANZ J Surg 2019; 89 (9): 385–387. DOI: 10.1111/ans.14559.
- Jorion JL, Michel M. Spontaneous rupture of bladder diverticula in a girl with Ehlers-Danlos syndrome. J Pediatr Surg 1999; 34 (3): 483–484. DOI: 10.1016/s0022-3468(99)90506-7.
- Temiz A, Akcora B, Atik E. An atypical bladder diverticulum presented with recurrent peritonitis: case report. Ulus Travma Acil Cerrahi Derg 2011; 17 (4): 365–367. DOI: 10.5505/tjtes.2011.81542.
- Christman MS, Casale P. Robot-Assisted Bladder Diverticulectomy in the Pediatric Population. J Endourol 2012; 26 (10): 1296–1300. DOI: 10.1089/end.2012.0051.
- Nerli RB, Ghagane SC, Musale A, Deole S, Hiremath MB, Dixit NS, et al.. Congenital bladder diverticulum in a child: Surgical steps of extra-vesical excision. Urol Case Rep 2019; 22: 42–43. DOI: 10.1016/j.eucr.2018.10.009.
- Cerwinka WH, Scherz HC, Kirsch AJ. Endoscopic Treatment of Vesicoureteral Reflux with Dextranomer/Hyaluronic Acid in Children. Adv Urol 2008; 2008: 1–7. DOI: 10.1155/2008/513854.
- Aydogdu O, Burgu B, Soygur T. Predictors of Surgical Outcome in Children With Vesicoureteral Reflux Associated With Paraureteral Diverticula. Urology 2010; 76 (1): 209–214. DOI: 10.1016/j.urology.2009.11.052.
Última actualización: 2025-09-21 13:35