28: 隐睾
阅读本章大约需要 6 分钟。
引言
未降睾丸(UDT)是指睾丸不位于阴囊,而位于异常部位,如腹腔或腹股沟内(图1)睾丸在胎儿期形成并在腹腔内停留一段时间,随后逐渐下降进入阴囊。隐睾症包括位于睾丸正常下降通道上任何部位的未降睾丸,以及不沿睾丸常规下降路径而位于异常位置的异位睾丸。未降睾丸应与回缩睾丸加以鉴别。回缩睾丸是指位于腹股沟外环以下、可被推送至阴囊上部且易回升至原位的睾丸,和/或指已完成正常下降过程、可以停留在阴囊内但在阴囊与腹股沟之间易来回移动的睾丸(视频1)。
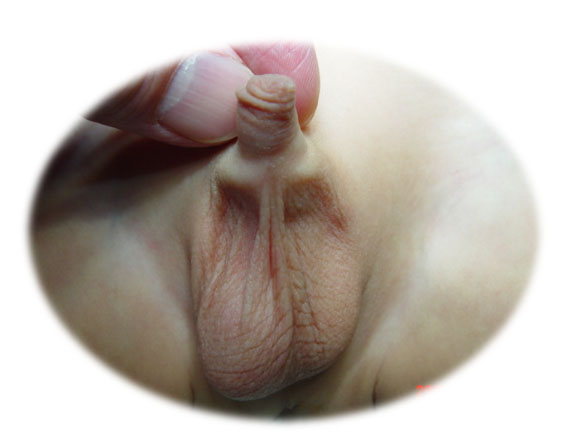
图 1 在隐睾患者中,左侧阴囊空虚。
视频 1 回缩性睾丸的演示。
流行病学
隐睾是男性新生儿最常见的先天异常之一。有隐睾同胞者的男性其发生隐睾的风险增加3.5倍,父亲患有该病者则增加2.3倍。1 据报道,足月新生儿的发生率为1.0–4.5%,单侧病例约为双侧病例的2倍。2 约70%的隐睾患儿在3个月龄时在小青春期的影响下可发生睾丸下降,至1岁时隐睾的发生率降至0.8-1.2%。3,4
病因
目前尚无明确的与隐睾(UDT)相关的危险因素;然而,孕期母亲吸烟、出生相关指标(包括出生体重和胎龄)、隐睾家族史,以及诸如INSL3突变等罕见遗传变异,均被认为与隐睾有关。正常的睾丸下降依赖于完整的下丘脑-垂体-性腺(HPG)轴。尽管其确切病因仍不清楚,但遗传因素、激素因素(HPG轴功能障碍、先天性性腺功能减退、睾丸发育不良)以及解剖学因素(输精管和精索血管过短)均被牵涉其中。出生体重<2.5 kg、小于胎龄儿、早产、母体雌激素水平低和胎盘功能不全、人绒毛膜促性腺激素(hCG)分泌减少等被认为是隐睾的危险因素。此外,持续暴露于有机氯化合物、邻苯二甲酸酯单酯、母体吸烟、母体糖尿病等环境因素已被报道为男性发育障碍的危险因素。然而,尚未发现其中任何因素可单独对隐睾的发病机制负责。
睾丸的正常下降
哺乳动物可分为具有阴囊者和无阴囊者。关于某些哺乳动物阴囊演化的一般假说认为:阴囊提供了一个低温环境,其温度低于核心体温,从而有利于精子发生。然而,我们缺乏支持或反驳这一温度假说的数据,因为一些哺乳动物在睾丸位于体内的情况下仍能繁殖,而一些无阴囊物种也具有睾丸降温机制。5,6 在较低体温下生殖细胞突变率降低,可能是哺乳动物阴囊演化的推动因素之一。某些动物的睾丸位于腹腔内、靠近肾脏,而其附睾延伸至皮下部位,这可能在精子储存和成熟过程中提供降温作用。7 在这种情况下,睾丸的位置可能随附睾的位置而变化。在人类中,阴囊温度维持在适于精子发生的最佳水平,约比核心体温低2.7 ℃。8
尽管睾丸和卵巢均起源于邻近肾脏的同一胚胎组织,睾丸却要经历一次离开腹腔的漫长迁移。9 正常的睾丸下降包括经腹阶段和腹股沟-阴囊阶段,两者均在人类的产前期发生。经腹下降发生于妊娠第12周,此时睾丸向深腹股沟环下移。其过程被认为是推动与牵拉相互交替作用的综合结果。10 在下降开始之前,发育中的性腺由颅侧悬韧带和尾侧生殖-腹股沟韧带(即引带,gubernaculum)固定。11 在经腹阶段,引带远端增大,使雄性引带变得短而粗厚。这种肿大反应将睾丸锚定于腹股沟管(图2) 腹股沟壁肌肉围绕肿大的引带(亦称球部)分化,形成腹股沟管。胰岛素样激素3(INSL3)被认为是该肿大反应的调节激素。12,13,14 睾丸的Leydig细胞分泌INSL3以刺激这种肿大反应,并在胎儿腹部增大时使睾丸保持靠近腹股沟腹壁。14 睾丸支持细胞分泌的抗苗勒管激素(AMH)也被认为在睾丸下降中发挥作用。AMH基因或其受体发生突变的儿童可出现隐睾,并伴持续存在的幼稚子宫和输卵管,称为持续性苗勒管综合征(PMDS)。14
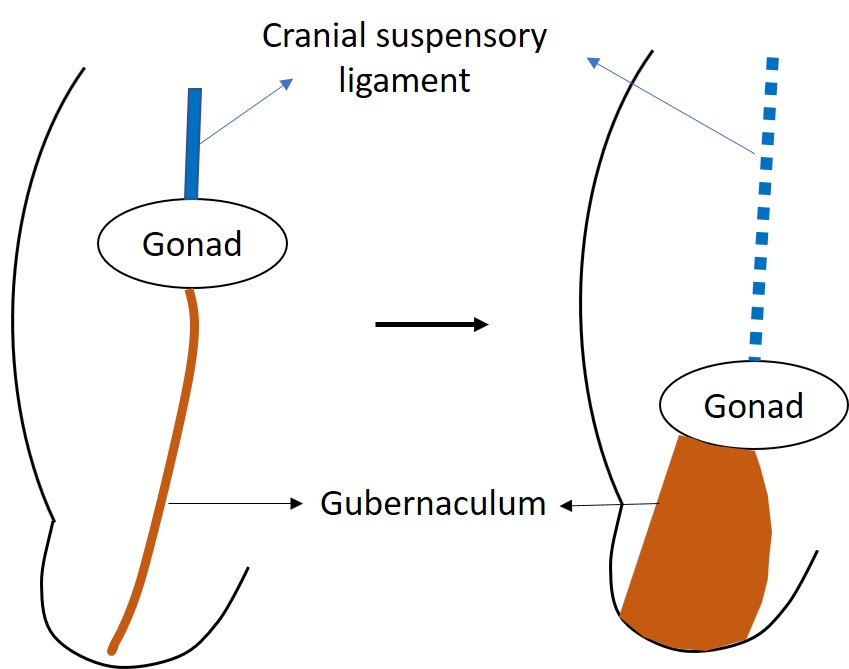
图 2 未分化的性腺最初位于腹部高位,由颅侧悬韧带固定。INSL3 促使睾丸引带肿胀并增大,从而将发育中的睾丸牵引向腹股沟区域。
腹股沟-阴囊期的下降发生在25至35周之间。整个过程在大多数哺乳动物中非常相似。15 在此阶段,睾丸穿过腹股沟管,最终位于阴囊内。引带随鞘状突一起向阴囊方向延长。引带到达阴囊后,其球状部被吸收,仅留下附着于阴囊内侧的纤维性残迹。鞘状突的近端闭合,以防止人类发生腹股沟疝或鞘膜积液。许多其他哺乳动物(如小鼠和大鼠)终生保留通畅的鞘状突。在人类中,鞘状突最终完全退化,并使精索在出生后能够正常延长。睾丸下降的腹股沟-阴囊期受雄激素控制。在动物模型中发现,取决于雄激素的作用,股生殖神经的感觉支控制引带的发育,而这种发育受降钙素基因相关肽(CGRP)调节。
隐睾的分类
一般而言,隐睾根据是否可触及分为可触及型或不可触及型。睾丸是否可触及决定了诊断检查与治疗策略,也影响预后。提睾肌的收缩可使睾丸移动。因此,最好在提睾反射较弱的6个月龄之前,或在全身麻醉下,确定睾丸的确切位置。约80%的隐睾在腹股沟区域可触及。若睾丸不可触及,可能位于腹腔内,或为先天性缺如、萎缩或消失性睾丸。
相关病理
生殖细胞发育异常
青春期前隐睾睾丸的组织学发育已在多种观察性研究中得到研究。这些研究提供了有力证据,显示隐睾睾丸在婴儿早期之后常存在生殖细胞发育异常。在隐睾睾丸以及程度较轻的对侧阴囊内睾丸中,婴儿期后每条小管内的精原细胞数量减少,且未能随年龄正常增加。16 据报道,隐睾睾丸中性母细胞向精原细胞的转化受损。在约1.5个月龄时,隐睾睾丸中性母细胞与精原细胞的比例似乎正常;与对侧阴囊内睾丸相比,隐睾睾丸中性母细胞的消失以及成人型暗精原细胞的出现均存在延迟。据报道,隐睾睾丸在出生时并不显著更小,但其生长不及阴囊内睾丸。17
不育症
众所周知,隐睾病史与生育力低下相关。在一系列关于隐睾生育力的设计良好的病例-对照研究中,分析了大量接受睾丸固定术的男性与年龄相仿的对照组,结果显示:既往双侧隐睾者中65%、既往单侧隐睾者中90%、对照组中93%成功生育。18,19 根据在进行睾丸固定术时报告睾丸组织学所见的研究,手术在1岁前进行时生育潜力最大。20,21,22 因此,建议在1岁前进行睾丸固定术。
恶性肿瘤风险
在有隐睾病史的男性中,发生睾丸生殖细胞肿瘤的风险众所周知会增加。未降睾发生恶性转化的相对风险总体为2.5至8,而在青春期前接受睾丸固定术的男孩中为2至3。23 约10%的睾丸生殖细胞肿瘤患者有隐睾病史。对已治疗与未治疗隐睾的肿瘤病理进行回顾时,精原细胞瘤最常见于持续隐睾的睾丸,而阴囊内睾丸则以非精原细胞性生殖细胞肿瘤为主。23 如今,这已被证明并无关联,推荐将睾丸自我检查用于睾丸癌筛查,并应在有隐睾病史的患者进入青春期后教授其进行自我检查。
疝气
超过90%的隐睾伴有腹膜鞘状突未闭,疝可发生于25%。
附睾异常
据报道,在隐睾症中附睾异常的发生率为32%至72%。24 附睾异常可能由于邻近正常睾丸的中肾管异常退行而发生。25 据报道,附睾-睾丸融合异常与睾丸更近端的位置密切相关。附睾异常可因精子运输与成熟困难而导致生育力受损。26
隐睾的诊断
在体格检查前,必须询问是否早产、母亲是否正在使用女性激素或曾接触女性激素、有无中枢神经系统病变以及既往腹股沟手术史。还应了解伴随隐睾症的其他先天畸形或不育的家族史。由于隐睾是否可触及比睾丸的位置更为重要,必须进行细致的体格检查。如有疑问,建议重复检查或转诊专科医生。尤其在睾丸不可触及时,术前在麻醉下检查非常重要。体格检查时房间需要温暖。令患儿取蛙式位,先检查对侧睾丸的大小、位置和表面,然后以温暖的手自患侧髂嵴向耻骨联合方向扫触,以确定睾丸的存在与位置。如能触及睾丸,还应检查其是否能下降至阴囊。27 若不易触及,如在胖乎乎的婴儿或肥胖儿童中,可令其盘腿坐位或下蹲位进行检查,并在手上涂抹润滑凝胶以便更好地触诊睾丸。若一侧睾丸缺如,可见对侧睾丸代偿性肥大。一旦睾丸可触及,则无需进一步检查,因为超声、计算机断层扫描或磁共振成像(MRI)的诊断准确性不如资深泌尿科医生,且影像学检查结果很少会改变治疗方案。影像学检查无法确切证实睾丸是否存在。28 在临床实践中,仅在可疑DSD患者的特定病例中建议行超声或MRI检查。29
对于在体格检查和影像学检查中无法证实的不可触及睾丸,可实施诊断性腹腔镜检查或经腹股沟或阴囊切口的探查手术。传统上,若经腹股沟探查发现睾丸或睾丸残迹,则随后行睾丸固定术或睾丸切除术。随着腹腔镜的出现,已能够评估睾丸是否存在、其位置,以及输精管和性腺血管的情况。腹腔镜下如见睾丸血管盲端终止,可诊断为消失性睾丸,无需进一步处理。若观察到精索血管进入腹股沟内环,则应进一步行腹股沟或阴囊探查。
在存在任何性发育差异(DSD)征象(如外生殖器不明确或重度尿道下裂)的双侧不可触及睾丸病例,必须进一步进行内分泌学和遗传学评估。30 对于3个月龄以下儿童,测定黄体生成素(LH)、促卵泡激素(FSH)和睾酮。对于≥3个月龄儿童,建议进行人绒毛膜促性腺激素(hCG)刺激试验。若睾酮几乎测不到且LH、FSH升高,可评估为无睾症。在hCG刺激试验中,肌肉注射2,000 IU的hCG,连续3天,于第5天测定血清睾酮。然而,鉴于可能出现假阴性,对于双侧睾丸均不可触及且促性腺激素水平在正常范围内的所有儿童,无论是否对hCG刺激试验有反应,均需进行手术确认。
隐睾症的治疗
治疗隐睾的目标是在早期将睾丸置入阴囊,尽量减少睾丸的组织学退变,从而降低不育风险;并且便于发现睾丸癌,而在隐睾中睾丸癌的发生率高于正常下降的睾丸。此外,次要目标是矫正伴随病变,预防睾丸扭转等并发症,减轻患者的心理影响,并改善美容外观。迄今普遍认为睾丸固定术不能预防睾丸癌,但近年来有报道显示,早期手术可降低睾丸癌风险。隐睾的治疗时机十分重要。睾丸固定术应在生后6个月之后并在随后一年内完成,最迟不应超过18个月。31 进行如此早期手术的依据在于:6个月之后睾丸自然下降的可能性很小,全身麻醉风险或手术技术并无显著差异,而且此年龄之后睾丸发生组织学损伤的可能性增加。31,32 另外,还担心18个月以上的儿童因手术而出现较强的分离焦虑和“被阉割”恐惧,从而影响儿童的心理健康。
手术治疗(睾丸固定术)是隐睾的标准治疗方式,并且可根据隐睾的位置和状况选择性使用激素治疗。当睾丸发生退化或消失,仅见睾丸残余或残端结节(nubbin)时,或成人隐睾在解剖结构和形态上异常时,或无法进行睾丸固定时,应行睾丸切除术。仅在对侧睾丸正常时方可谨慎决定行睾丸切除术,并同时对对侧行睾丸固定术以预防睾丸扭转。由于回缩睾属于正常变异,建议每年随访,直至青春期或直至睾丸不再上移。
促睾丸下降的激素治疗
用于促进睾丸下降的激素治疗仍然存在争议。然而,主要使用hCG、促黄体生成素释放激素(LHRH)激动剂或促性腺激素释放激素(GnRH)激动剂。开展激素治疗的依据来自实验结果:未降睾丸源于下丘脑–垂体–性腺轴的异常,睾丸下降受男性雄激素调控,且在睾丸内合成的活性代谢物的高浓度参与隐睾的发病机制。hCG如同垂体分泌的LH一样直接作用于Leydig细胞,而GnRH则通过下丘脑刺激促使分泌LH,从而增加睾丸的睾酮生成。据推测,这些激素通过影响精索和提睾肌来诱导睾丸自然下降并提高生育力。然而,采用hCG或GnRH进行激素治疗的成功率仅为20%,且其中近20%的已下降睾丸随后可能再次上移。33,34
生育力的激素治疗
激素治疗可能改善生育指标,并可作为睾丸固定术的辅助治疗。35,36 有报道显示,儿童期接受促性腺激素释放激素(GnRH)治疗的男性,其精液分析结果优于仅行睾丸固定术或安慰剂治疗者。35 相反,有报道指出,人绒毛膜促性腺激素(hCG)治疗可能通过增加生殖细胞凋亡、引起睾丸的炎性改变以及导致成年后睾丸体积减小而对未来的精子发生不利。37 关于隐睾症激素治疗的长期效果证据仍然不足,且难以筛选出最可能从激素治疗中获益的隐睾患者。
手术治疗
可触及睾丸
在大多数可触及的隐睾病例中,睾丸固定术通过腹股沟切口实施。睾丸固定术中最重要的一点是获得足够的长度,使睾丸在无张力的情况下下降至阴囊。手术包括以下四个步骤。首先,将睾丸及精索与周围组织分离,以获得活动度。其次,对鞘状突进行高位结扎以予关闭。第三,为在无张力情况下将睾丸下降至阴囊底部,有时需要进一步进行腹膜后分离以游离输精管。最后,在同侧阴囊建立浅表达尔托肌下囊袋,将睾丸置入并固定。如果采用这些基础技术仍无法获得足够的精索长度,则需要行Prentiss法,通过在腹股沟管底部切断下腹壁血管,或使精索自其下方通过,以缩短至阴囊的距离。对于可触及的隐睾并非常规采用,亦有报道使用显微外科技术将睾丸动脉与腹壁动脉行吻合以进行睾丸自体移植(见下文)。
不可触及睾丸
由于在处理不可触及性睾丸的手术中,睾丸的存在及状态至关重要,应在麻醉下再次检查睾丸。若仍不可触及,则行开放性腹股沟探查或诊断性腹腔镜检查。不可触及睾丸在腹腔镜下的所见包括:首先,精索血管经腹股沟内环向下走行。此时在腹股沟或阴囊皮肤切开以探查睾丸是否存在;若发现睾丸正常,则进行睾丸固定术。第二种情况为精索血管在靠近腹股沟内环的腹腔内终止于盲端,提示消失性睾丸,因此停止手术,不再进一步手术。最后,当在腹腔内发现睾丸时,手术决策依据睾丸大小、其在腹腔内的位置、精索血管长度、患儿年龄、对侧睾丸情况以及术者经验综合制定。总体手术成功率已知为67-84%。
睾丸固定术可通过三种方式之一实施
Fowler-Stephens 睾丸固定术
这是一种通过切除包含睾丸动脉的内精索血管以确保精索长度的手术,睾丸的存活依赖于提睾肌动脉和输精管动脉的血供。单期技术是在切除内精索血管的同时对睾丸进行固定的方法。在两期Fowler-Stephens睾丸固定术中,首先将内精索血管作为一期手术予以结扎,使来自腹腔至睾丸的侧支血供在至少6个月内增加,随后通过二期手术将睾丸降至阴囊。单期或两期的Fowler-Stephens睾丸固定术可采用腹腔镜方式实施。
腹腔镜下睾丸固定术
由于腹腔镜手术是在放大视野下进行,因此在进行广泛游离的同时,具有尽量减少血管损伤并确保睾丸动员最短路径的优势 (图3) 和 (视频1)。腹腔镜睾丸固定术包括在保留内精索血管的情况下将睾丸下降至阴囊的方法以及 Fowler-Stephens 方法 (视频2)。借助腹腔镜,可进行显微外科自体移植术。
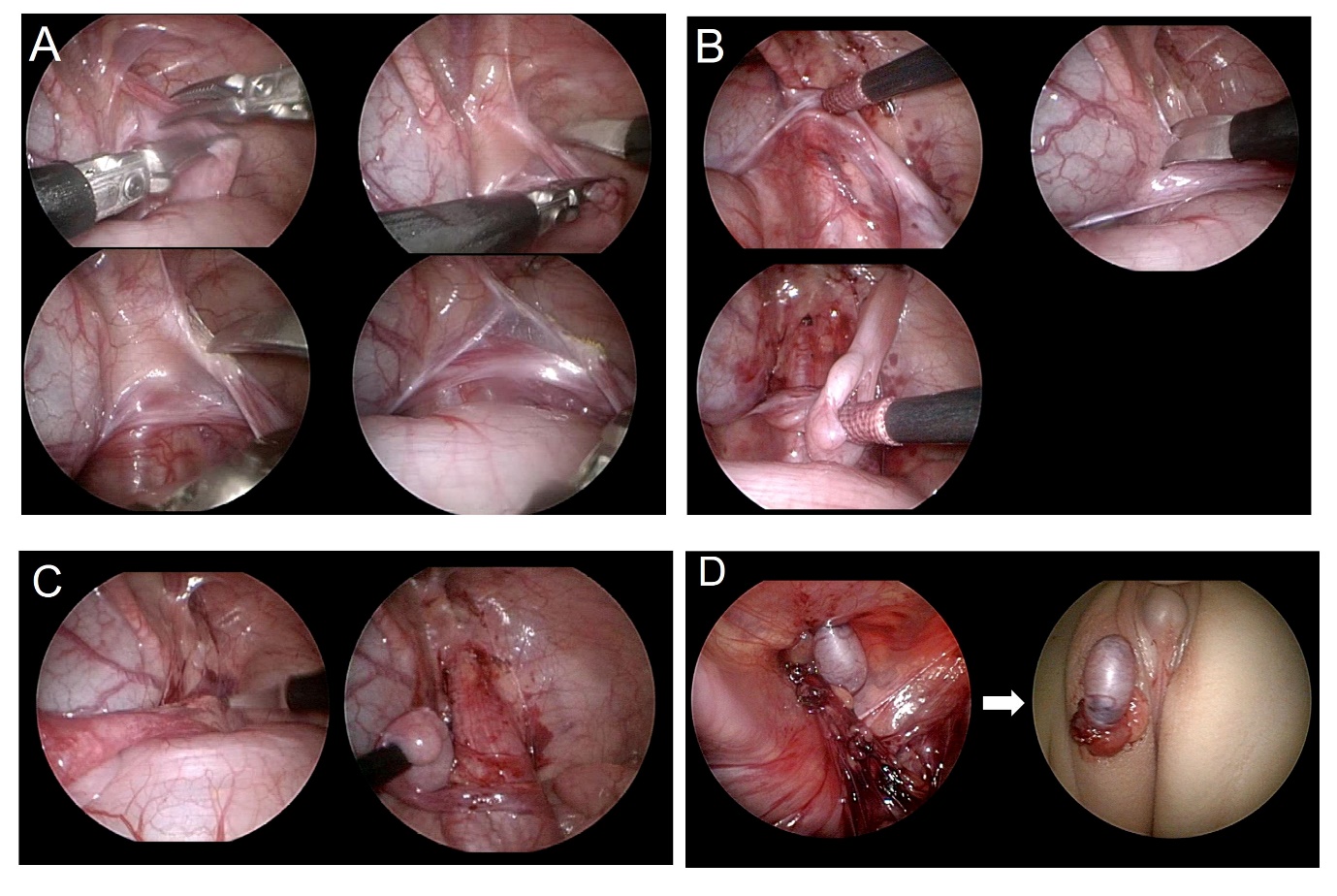
图 3 腹腔镜睾丸固定术的分步示意图。(A) 切断睾丸引带,(B) 沿输精管方向游离腹膜,(C) 沿睾丸血管方向切开腹膜,(D) 建立新裂孔并将睾丸从腹腔牵出至阴囊位置。
视频 2 Fowler-Stephens 睾丸固定术演示。
使用显微外科进行自体移植
这在睾丸位于腹腔深处的特殊情况下实施。首先,将睾丸及精索予以游离并固定于阴囊内,随后通过显微外科将睾丸血管与下腹壁血管进行吻合,以重新开通血流。尽管其成功率相对较高,但由于显微血管吻合对技术与投入要求很高,且需要细致的术后管理,因此并非易于选择的方法。
睾丸切除术
当因严重睾丸萎缩或形态学异常而预期无睾丸功能时,进行睾丸切除术。
睾丸固定术的并发症和再手术
睾丸固定术的并发症包括睾丸回缩、血肿、髂腹股沟神经损伤、精索扭转、输精管损伤或睾丸萎缩。睾丸萎缩是最严重的并发症,多发生于对精索过度游离或电凝使用过度、精索血管扭曲,或在进行 Fowler-Stephens 睾丸固定术时在张力下强行下牵睾丸,致血供受影响。睾丸回缩通常由于腹膜后游离不充分所致,睾丸被牵拉至阴囊以上,位于腹股沟外环下方或耻骨结节附近。再次手术时,应避开既往手术部位另行切开,从正常组织进入瘢痕组织,去除包含正常组织在内的坚硬瘢痕组织,以免精索血管受损,随后进行睾丸固定术。
要点
- AUA 隐睾指南 指出,隐睾(UDT)的手术最好在1岁之前进行
- Choosing Wisely 倡议与 AUA 合作决定强调,对隐睾(UDT)不应常规进行影像学检查,因为确认睾丸位置最好通过体格检查完成;若为不可触及睾丸,必要时可行腹腔镜检查。
- 经腹股沟或阴囊入路的睾丸固定术成功率高、并发症发生率低
- 腹腔镜睾丸固定术与更高的睾丸萎缩发生率相关
参考文献
- Hutson JM, Balic A, T N. Cryptorchidism. Semin Pediatr Surg 2010; 19: 215. DOI: 10.1002/bjs.1800760203.
- Ashley RA, JS B, Kolon TF. Cryptorchidism: pathogenesis, diagnosis, treatment and prognosis. Urol Clin North Am 2010; 37: 183. DOI: 10.1016/j.ucl.2010.03.002.
- Elder JS. The undescended testis. Hormonal and Surgical Management Surg Clin North Am 1988; 68: 983. DOI: 10.1515/iupac.88.1460.
- Sijstermans K, Hack WW, RW M. The frequency of undescended testis from birth to adulthood: a review. Int J Androl 2008; 31: 1. DOI: 10.1111/j.1365-2605.2008.00883.x.
- Werdelin L, Nilsonne A. The evolution of the scrotum and testicular descent in mammals: a phylogenetic view. J Theor Biol 1999; 196: 61. DOI: 10.1006/jtbi.1998.0821.
- Lovegrove BG. Cool sperm. why some placental mammals have a scrotum. J Evol Biol 2014; 27: 801. DOI: 10.1111/jeb.12373.
- Bedford JM. Anatomical evidence for the epididymis as the prime mover in the evolution of the scrotum. Am J Anat 1978; 152: 483. DOI: 10.1002/aja.1001520404.
- Momen MN, Ananian FB, IM F. Effect of high environmental temperature on semen parameters among fertile men. Fertil Steril 2010; 93: 1884. DOI: 10.1016/j.fertnstert.2008.12.065.
- Hutson JM, S H, Heyns CF. Anatomical and functional aspects of testicular descent and cryptorchidism. Endocr Rev 1997; 18: 259. DOI: 10.1210/er.18.2.259.
- Costa WS, Sampaio FJ, LA F. Testicular migration: remodeling of connective tissue and muscle cells in human gubernaculum testis. J Urol 2002; 167: 2171. DOI: 10.1097/00005392-200205000-00065.
- P S, W E. Perinatal development of gubernacular cones in rats and rabbits: effect of exposure to anti-androgens. Anat Rec 1993; 236: 399. DOI: 10.1002/ar.1092360214.
- Nef S, Parada LF. Cryptorchidism in mice mutant for Insl3. Nat Genet 1999; 22: 295. DOI: 10.1038/10364.
- Zimmermann S, Steding G, JM E. Targeted disruption of the Insl3 gene causes bilateral cryptorchidism. Mol Endocrinol 1999; 13: 681. DOI: 10.1210/mend.13.5.0272.
- Hutson JM, Li R, BR S. Regulation of testicular descent. Pediatr Surg Int 2015; 31: 317. DOI: 10.1007/s00383-015-3673-4.
- Hutson JM, Baskin LS, G R. The power and perils of animal models with urogenital anomalies: handle with care. J Pediatr Urol 2014; 10: 699. DOI: 10.1016/j.jpurol.2014.03.003.
- Gracia J, Sanchez Zalabardo J, J SG. Clinical, physical, sperm and hormonal data in 251 adults operated on for cryptorchidism in childhood. BJU Int 2000; 85: 1100. DOI: 10.1046/j.1464-410x.2000.00662.x.
- Kollin C, Hesser U, EM R. Testicular growth from birth to two years of age, and the effect of orchidopexy at age nine months: a randomized, controlled study. Acta Paediatr 2006; 95: 318. DOI: 10.1080/08035250500423812.
- Miller KD, MT C, Lee PA. Fertility after unilateral cryptorchidism. Paternity, time to conception, pretreatment testicular location and size, hormone and sperm parameters. Horm Res 2001; 55: 249.
- Lee PA, Coughlin MT. Fertility after bilateral cryptorchidism. Evaluation by paternity, hormone, and semen data. Horm Res 2001; 55: 28.
- Park KH, Lee JH, JJ H. Histological evidences suggest recommending orchiopexy within the first year of life for children with unilateral inguinal cryptorchid testis. Int J Urol 2007; 14: 616. DOI: 10.1111/j.1442-2042.2007.01788.x.
- Kogan SJ, Tennenbaum S, B G. Efficacy of orchiopexy by patient age 1 year for cryptorchidism. J Urol 1990; 144: 508. DOI: 10.1016/s0022-5347(17)39505-8.
- Tasian GE, Hittelman AB, GE K. Age at orchiopexy and testis palpability predict germ and Leydig cell loss: clinical predictors of adverse histological features of cryptorchidism. J Urol 2009; 182: 704. DOI: 10.1590/s1677-55382009000500033.
- Wood HM, Elder JS. Cryptorchidism and testicular cancer: separating fact from fiction. J Urol 2009; 181: 452. DOI: 10.1016/s0084-4071(09)79277-2.
- Caterino S, Lorenzon L, M C. Epididymal-testicular fusion anomalies in cryptorchidism are associated with proximal location of the undescended testis and with a widely patent processus vaginalis. J Anat 2014; 225: 473. DOI: 10.1111/joa.12222.
- Mollaeian M, V M, Elahi B. Significance of epididymal and ductal anomalies associated with undescended testis: study in 652 cases. Urology 1994; 43: 857. DOI: 10.1016/0090-4295(94)90152-x.
- Kim SO, Na SW, HS Y. Epididymal anomalies in boys with undescended testis or hydrocele: Significance of testicular location. BMC Urol 2015; 15: 108. DOI: 10.1186/s12894-015-0099-1.
- Cendron M, Huff DS, MA K. Anatomical, morphological and volumetric analysis: a review of 759 cases of testicular maldescent. J Urol 1993; 149: 570. DOI: 10.1016/s0022-5347(17)36151-7.
- Hrebinko RL, Bellinger MF. The limited role of imaging techniques in managing children with undescended testes. J Urol 1993; 150: 458. DOI: 10.1016/s0022-5347(17)35510-6.
- Tasian GE, Copp HL. Diagnostic performance of ultrasound in nonpalpable cryptorchidism: a systematic review and meta-analysis. Pediatrics 2011; 127: 119. DOI: 10.1016/j.yuro.2011.05.011.
- Elert A, Jahn K, A H. Population-based investigation of familial undescended testis and its association with other urogenital anomalies. J Pediatr Urol 2005; 1: 403. DOI: 10.1016/j.jpurol.2005.04.005.
- Engeler DS, Hosli PO, H J. Early orchiopexy: prepubertal intratubular germ cell neoplasia and fertility outcome. Urology 2000; 56: 144. DOI: 10.1016/s0090-4295(00)00560-4.
- Wenzler DL, DA B, Park JM. What is the rate of spontaneous testicular descent in infants with cryptorchidism? J Urol 2004; 171: 849. DOI: 10.1097/01.ju.0000106100.21225.d7.
- Pyorala S, NP H, Uhari M. A review and meta-analysis of hormonal treatment of cryptorchidism. J Clin Endocrinol Metab 1995; 80: 2795. DOI: 10.1210/jc.80.9.2795.
- Rajfer J, Walsh PC. The incidence of intersexuality in patients with hypospadias and cryptorchidism. J Urol 1976; 116: 769. DOI: 10.1016/0022-3468(77)90475-4.
- Hagberg S, Westphal O. Treatment of undescended testes with intranasal application of synthetic LH-RH. Eur J Pediatr 1982; 139: 285. DOI: 10.1007/bf00442181.
- Hadziselimovic F, Herzog B. Treatment with a luteinizing hormone-releasing hormone analogue after successful orchiopexy markedly improves the chance of fertility later in life. J Urol 1997; 158: 1193. DOI: 10.1097/00005392-199709000-00132.
- Cortes D, J T, Visfeldt J. Hormonal treatment may harm the germ cells in 1 to 3-year-old boys with cryptorchidism. J Urol 2000; 163: 1290. DOI: 10.1097/00005392-200004000-00070.
最近更新时间: 2025-09-22 08:00